题目内容
下列储存药品的方法中,正确的是( )
| A、金属钠保存在水中 |
| B、烧碱溶液保存在玻璃塞试剂瓶中 |
| C、金属钠保存在无水乙醇中 |
| D、浓硝酸可贮存在铝制容器中 |
考点:化学试剂的存放
专题:
分析:A、钠和水反应生成氢氧化钠和氢气;
B、烧碱可与玻璃中的二氧化硅反应;
C、乙醇与钠反应生成乙醇钠和氢气;
D、浓硝酸见光易分解.
B、烧碱可与玻璃中的二氧化硅反应;
C、乙醇与钠反应生成乙醇钠和氢气;
D、浓硝酸见光易分解.
解答:
解:A、钠能分别与水和氧气等反应,钠的密度比水的小比煤油的大,所以少量的金属钠应保存在煤油中,隔绝空气,不能保存在水中,故A错误;
B、NaOH与二氧化硅反应生成的硅酸钠具有粘合性,则不能使用玻璃塞,所以NaOH溶液盛放在带橡皮塞的细口瓶中,故B错误;
C、钠能与乙醇反应,钠的密度比水的小比煤油的大,所以少量的金属钠应保存在煤油中,隔绝空气,不能保存在乙醇中,故C错误;
D、浓硝酸见光易分解,应放在棕色试剂瓶中避光保存,故D正确;
故选D.
B、NaOH与二氧化硅反应生成的硅酸钠具有粘合性,则不能使用玻璃塞,所以NaOH溶液盛放在带橡皮塞的细口瓶中,故B错误;
C、钠能与乙醇反应,钠的密度比水的小比煤油的大,所以少量的金属钠应保存在煤油中,隔绝空气,不能保存在乙醇中,故C错误;
D、浓硝酸见光易分解,应放在棕色试剂瓶中避光保存,故D正确;
故选D.
点评:本题考查试剂的存放,明确物质的性质与保存方法的关系是解答本题的关键,熟悉硝酸、二氧化硅、钠的性质即可解答,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
在下列各组溶液中,离子一定能大量共存的是( )
| A、加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I- |
| B、通入SO2气体后的溶液:Na+、Ca2+、K+、Cl- |
| C、0.1 mol?L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- |
| D、1mol/LNH4Al(SO4)2的溶液:K+、Ca2+、HCO3-、Cl- |
氯菊酯属低毒杀虫剂结构如图所示,下列有关氯菊酯说法正确的是( )
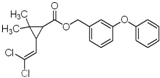

| A、分子式为C21H20Cl2O3 |
| B、不能使溴水褪色 |
| C、1mol氯菊酯与氢气加成最多消耗8 mol H2 |
| D、与NaOH溶液反应最多消耗4mol NaOH |
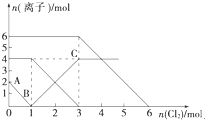 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2=2Fe3++2Br-2Fe3++2I-=2Fe2++I2,则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2=2Fe3++2Br-2Fe3++2I-=2Fe2++I2,则下列有关说法中,不正确的是( )| A、还原性:I->Fe2+>Br- |
| B、原混合溶液中FeBr2的物质的量为3 mol |
| C、当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl- |
| D、原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
下列说法不正确的是( )
| A、向AlCl3溶液中滴加氨水,产生白色沉淀,再加入盐酸,沉淀消失 |
| B、向铜粉中加入稀硫酸,铜粉不溶解,再加入Cu(NO3)2固体,铜粉溶解 |
| C、向BaCl2溶液中加入Na2SO3溶液,产生沉淀,再加入硝酸,沉淀全部溶解 |
| D、向盛有FeCl2溶液的试管中滴加NaOH溶液,最终生成红褐色的Fe(OH)3沉淀 |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入1.60g CuO,恰好恢复到电解前的浓度和pH.则电解过程中转移电子的总物质的量为( )
| A、0.02mol |
| B、0.04mol |
| C、0.06mol |
| D、0.08mol |
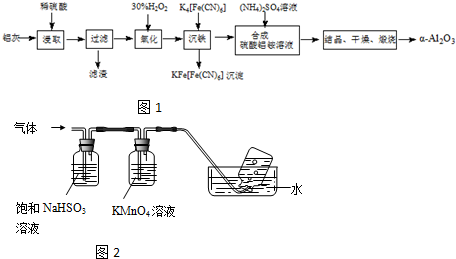
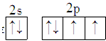 ,它的单质常温时为气态.试用化学符号回答以下问题.
,它的单质常温时为气态.试用化学符号回答以下问题.