题目内容
已知在10℃时Na2CO3的溶解度为29g,NaHCO3的溶解度为8g.在常温下,将0.5mol的Na2CO3溶于200g水中,然后通入过量的CO2,再冷却到10℃时,最后会析出晶体 g.
考点:溶液中溶质的质量分数及相关计算
专题:物质的量浓度和溶解度专题
分析:溶解度是指在一定温度下,100克溶剂中最多溶解的这种物质的质量;
Na2CO3 +H2O+CO2 =2NaHCO3,故0.5mol的Na2CO3与过量的CO2反应生成碳酸氢钠的质量为:84×0.5×2=84g,反应的水的质量为:18×0.5=9g,再根据溶解度进行计算.
Na2CO3 +H2O+CO2 =2NaHCO3,故0.5mol的Na2CO3与过量的CO2反应生成碳酸氢钠的质量为:84×0.5×2=84g,反应的水的质量为:18×0.5=9g,再根据溶解度进行计算.
解答:
解:Na2CO3 +H2O+CO2 =2NaHCO3,故0.5mol的Na2CO3与过量的CO2反应生成碳酸氢钠的质量为:84×0.5×2=84g,反应的水的质量为:18×0.5=9g,故10℃时,溶解的碳酸氢钠的质量为:
×8=15.36g,故最后会析出晶体的质量为84-15.36=68.64g,
故答案为:68.64.
| 200-9 |
| 100 |
故答案为:68.64.
点评:本题考查溶解度的相关计算,难度中等.侧重培养学生的分析能力和计算能力.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
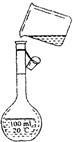 某同学在实验中需配制250ml 0.1mol/L NaCl溶液,如图为该学生转移溶液的示意图,图中的错误有( )
某同学在实验中需配制250ml 0.1mol/L NaCl溶液,如图为该学生转移溶液的示意图,图中的错误有( )| A、1处 | B、2处 | C、3处 | D、4处 |
现有两种只含C、H两种元素的有机物混合气体0.1mol,完全燃烧生成0.12molCO2和0.2molH2O,则该混合气体中( )
| A、一定含有甲烷 |
| B、一定含有乙烯 |
| C、可能含有甲烷 |
| D、不能确定 |
下列说法正确的是( )
A、按系统命名法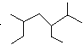 的名称为2-甲基-3,5-二乙基己烷 的名称为2-甲基-3,5-二乙基己烷 |
| B、用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯、硝基苯四种物质 |
| C、若两种二肽互为同分异构体,则二者的水解产物一定不相同 |
| D、等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次增加 |
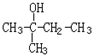 此化合物在浓硫酸作用下发生消去反应,写出所有可能的有机产物的结构简式:
此化合物在浓硫酸作用下发生消去反应,写出所有可能的有机产物的结构简式: