题目内容
在一定温度下,将2molA和2molB两种气体混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)X的值等于 ;
(2)B的平衡浓度为 ;
(3)A的转化率为 ;
(4)生成D的反应速率为 ;
(5)如果增大反应体系的压强,则平衡体系中C的质量分数 (填“增大”、“减小”或“不变”)
(6)如果上述反应在相同的条件下从逆反应开始进行,开始加入C和D各
mol,要使平衡时各物质的质量分数与原平衡时完全相同,则还应加入 mol 物质.
(1)X的值等于
(2)B的平衡浓度为
(3)A的转化率为
(4)生成D的反应速率为
(5)如果增大反应体系的压强,则平衡体系中C的质量分数
(6)如果上述反应在相同的条件下从逆反应开始进行,开始加入C和D各
| 4 |
| 3 |
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)C表示的反应速率为0.2mol/(L?min),平衡时C的浓度为0.4mol/L,则n(C)=0.4mol/L×2L=0.8mol,结合n(D)利用物质的量之比等于化学计量数之比计算x;
(2)浓度c=
计算得到;
(3)根据平衡时n(D),由方程式可知参加反应的n(A)=
n(D),再根据转化率定义计算A的转化率;
(4)反应速率v=
计算反应速率得到;
(5)若反应前后气体的物质的量不变,增大压强,平衡不移动,平衡体系中C的质量分数不变;若反应前后气体的物质的量变化,增大压强平衡向气体物质的量减小的分析移动,气体的总质量不变,据此判断;
(6)由(1)可知反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,据此判断应加入的物质及该物质的量物质的量.
(2)浓度c=
| n |
| V |
(3)根据平衡时n(D),由方程式可知参加反应的n(A)=
| 3 |
| 2 |
(4)反应速率v=
| △c |
| △t |
(5)若反应前后气体的物质的量不变,增大压强,平衡不移动,平衡体系中C的质量分数不变;若反应前后气体的物质的量变化,增大压强平衡向气体物质的量减小的分析移动,气体的总质量不变,据此判断;
(6)由(1)可知反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,据此判断应加入的物质及该物质的量物质的量.
解答:
解:(1)以C表示的反应速率为0.2mol/(L?min),平衡时C的浓度为0.4mol/L,则n(C)=0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,所以0.8mol:0.8mol=x:2,解得x=2,
故答案为:2;
(2)B的平衡浓度=
=0.8mol/L;
故答案为:0.8mol/L;
(3)平衡时n(D)=0.8mol,由方程式可知参加反应的n(A)=
n(D)=×0.8mol=1.2mol,故A的转化率为
×100%=60%,故答案为:60%;
(4)生成D的反应速率=
=0.2mol/L?min;
故答案为:0.2mol/L?min;
(5)反应前后气体的物质的量不变,增大压强,平衡不移动,平衡体系中C的质量分数不变,
故答案为:不变;
(6)该反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,开始加入C和D各
mol,由化学方程式3A(g)+B(g)?2C(g)+2D(g)可知转化到左边,可以得到A为
mol×
=2mol,得到B为
mol×
=
mol,故还需要加入B,加入B的物质的量为2mol-
mol=
mol;
故答案为:
;B;
故答案为:2;
(2)B的平衡浓度=
| 2mol-0.4mol |
| 2L |
故答案为:0.8mol/L;
(3)平衡时n(D)=0.8mol,由方程式可知参加反应的n(A)=
| 3 |
| 2 |
| 1.2mol |
| 2mol |
(4)生成D的反应速率=
| ||
| 2min |
故答案为:0.2mol/L?min;
(5)反应前后气体的物质的量不变,增大压强,平衡不移动,平衡体系中C的质量分数不变,
故答案为:不变;
(6)该反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,开始加入C和D各
| 4 |
| 3 |
| 4 |
| 2 |
| 3 |
| 2 |
| 4 |
| 3 |
| 1 |
| 2 |
| 2 |
| 3 |
| 2 |
| 3 |
| 4 |
| 3 |
故答案为:
| 4 |
| 3 |
点评:本题考查化学平衡的有关计算、影响化学平衡的因素、等效平衡等,难度中等,注意等效平衡规律的掌握.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
铝的活泼性较强,直到18世纪人类才开始将Al从它的化合物中冶炼出来.当时铝价格十分昂贵,拿破仑的头盔就是用Al制作的,现在还保存在英国博物馆中.电解熔融的氧化铝(冰晶石作助熔剂)时,当电路中通过10mol电子时,理论上析出铝的质量是( )
| A、90g | B、180g |
| C、270g | D、540g |
短周期元素Q、R、T、W在元素周期表中的位置如下图所示,其中T所处的周期序数与主族序数相等,下列推测正确的是 ( )
| Q | R | ||
| T | W |
| A、Q形成的化合物的种类最多 |
| B、T位于元素周期表的第三周期第III族 |
| C、Q和R的气态氢化物,前者比后者稳定 |
| D、原子及简单离子半径均是T>W |
欲使CaCl2与盐酸的混合溶液中和至中性且得到CaCl2溶液,在不用指示剂的情况下,最好选用的物质是( )
| A、氨水 |
| B、碳酸钠 |
| C、CaCO3 |
| D、氧化钙 |
下列除去杂质所选用的试剂正确的是( )
| A、除去N2中混有的O2:选用灼热的铜网 |
| B、除去CO2中混有的CO:选用澄清石灰水 |
| C、除去BaCO3固体中混有的BaSO4:选用稀硫酸 |
| D、除去Cu粉中混有的CuO:选用稀盐酸 |
氨水有下列平衡NH3.H2O?NH4++OH-,当其它条件不变时,改变下列条件,平衡向左移,且c(NH4+)增大的是( )
| A、加NaOH |
| B、加盐酸 |
| C、加NH4Cl |
| D、加同浓度氨水 |
 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A、反应的化学方程式5Y?X |
| B、t1时,Y的浓度是X浓度的1.5倍 |
| C、t2时,正、逆反应速率相等 |
| D、t3时,增大压强,v(正)增大,v(逆)减小 |
将标况下的2.24LCO2通入150mL 1mol?L-1NaOH溶液中,下列说法正确的是( )
| A、c(HCO3-) 略大于c(CO32-) |
| B、c(HCO3-) 等于c(CO32-) |
| C、c(Na+)等于c(CO32-)与c(HCO3-)之和 |
| D、c(HCO3-) 略小于c(CO32-) |
向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断不正确的是( )(不计CO2的溶解)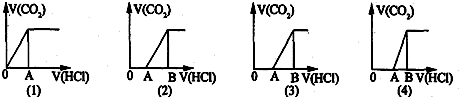

| A、M中只有一种溶质的有(1)和(3) |
| B、M中有两种溶质的有(2)和(4) |
| C、(2)图显示M中c(NaHCO3)<c(Na2CO3) |
| D、(4)图显示M中的溶质为NaOH和Na2CO3 |