题目内容
5.将碳酸钠和碳酸氢钠分别加热,可发生分解反应的是NaHCO3,反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.鉴别碳酸钠和碳酸氢钠的溶液,可用氯化钙溶液,碳酸钠与之反应产生白色沉淀,反应的离子方程式Ca2++CO32-=CaCO3↓,碳酸氢钠不反应.分析 碳酸氢钠不稳定,加热易分解,生成碳酸钠、水和二氧化碳,鉴别碳酸钠和碳酸氢钠的溶液,可加入氯化钙溶液,碳酸钠与氯化钙反应生成碳酸钙沉淀,碳酸氢钠不反应,以此解答该题.
解答 解:碳酸氢钠不稳定,加热易分解,生成碳酸钠、水和二氧化碳,反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,鉴别碳酸钠和碳酸氢钠的溶液,可加入氯化钙溶液,碳酸钠与氯化钙反应生成碳酸钙沉淀,反应的离子方程式为Ca2++CO32-=CaCO3↓,碳酸氢钠不反应,
故答案为:NaHCO3;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;Ca2++CO32-=CaCO3↓.
点评 本题考查碳酸钠和碳酸氢钠等知识,为高频考点,侧重考查学生对双基知识的掌握,难度不大,注意碳酸氢钠的不稳定性以及鉴别二者的方法.

练习册系列答案
相关题目
15.煤的气化是实施节能环保的一项重要措施.通常在高温下将煤转化为水煤气,再将水煤气作为气体燃料.有关热化学方程式如下:
①C(s)+H2O(g)═CO(g)+H2(g)△H1=+131.3kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1.
下列有关说法正确的是( )
①C(s)+H2O(g)═CO(g)+H2(g)△H1=+131.3kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1.
下列有关说法正确的是( )
| A. | 水煤气只能用作燃料 | |
| B. | 水煤气是一种二级能源,比煤直接燃烧污染小 | |
| C. | 等质量的CO和H2完全燃烧时,前者放热多 | |
| D. | 由③反应可以确定H2的燃烧热为241.8 kJ•mol-1 |
13.据报道,科学家已成功合成了少量N4,有关N4的说法正确的是( )
| A. | N4和N2是氮元素的两种不同单质 | |
| B. | ${\;}_{7}^{14}{N}_{4}$、${\;}_{7}^{15}{N}_{2}$互为同位素 | |
| C. | 相同质量的N4和N2所含原子个数比为1:2 | |
| D. | ${\;}_{7}^{14}{N}_{4}$的摩尔质量是56g/mol |
20.如果把12C的相对原子质量定义为24,以0.024 kg12C所含的C原子数为阿伏加德罗常数,在标准状况时下列数值肯定不变的是( )
| A. | 浓硫酸(98%)的物质的量浓度 | B. | 常温下氯化钠的溶解度 | ||
| C. | 标准状况下气体摩尔体积 | D. | 0.2g金刚石所含的C原子数 |
10.化学是一门充满神奇色彩的科学.下列说法正确的是( )
| A. | 按分散系中分散质粒子的大小可以把分散系分为溶液、胶体和浊液 | |
| B. | 氧化还原反应的本质是化合价的升降 | |
| C. | 金属的硬度都比较大,不能用刀切 | |
| D. | 氯气常用做自来水的净水剂,原因是氯气无毒,对人体无害 |
17.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 mol Cu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 标准状况下,22.4 L Cl2含NA个原子 | |
| D. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 |
14.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4•7H2O),设计了如图流程:下列说法不正确的是( )
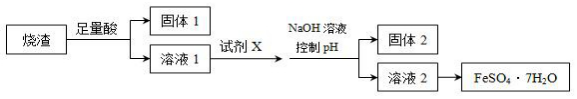

| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH为使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
15.氯苯是燃料、医药、有机合成的中间体,是重要的有机化工产品.实验室制取氯苯如图1所示(加热和固定仪器的装置略去).
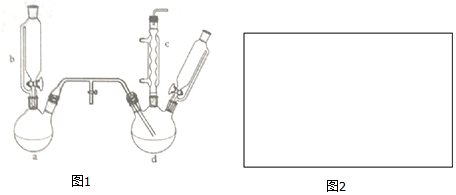
回答下列问题:
(1)a和b仪器组合成制取氯气的装置,反应无需加热,则a装置中的固体反应物可以是BC.(填序号)
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)把氯气通入反应器d中(d装置有FeCl3和苯),加热维持反应温度40-60℃,温度过高会生成过多的二氯苯.对d加热的方法是水浴加热.
(3)装置c的名称是(球形)冷凝管,装置c出口的气体成分有HCl、Cl2、水蒸气和苯蒸汽.
(4)制取氯苯的化学方程式为: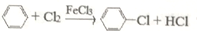 .
.
(5)装置d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.
①碱洗之前要水洗.其目的是洗去FeCl3、HCl等无机物.节省碱的用量,降低成本.
②10%NaOH溶液碱洗时发生氧化还原反应的化学反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.
(6)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸汽,请在图2中画出,并标明所用试剂.
(7)工业生产中苯的流失情况如表所示:
则10t 苯可制得成品氯苯$\frac{10×(1-0.0892)×112.5}{78}$t.(列出计算式即可.氯苯和苯的相对分子质量分别是112,5和78)

回答下列问题:
(1)a和b仪器组合成制取氯气的装置,反应无需加热,则a装置中的固体反应物可以是BC.(填序号)
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)把氯气通入反应器d中(d装置有FeCl3和苯),加热维持反应温度40-60℃,温度过高会生成过多的二氯苯.对d加热的方法是水浴加热.
(3)装置c的名称是(球形)冷凝管,装置c出口的气体成分有HCl、Cl2、水蒸气和苯蒸汽.
(4)制取氯苯的化学方程式为:
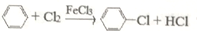 .
.(5)装置d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏.
①碱洗之前要水洗.其目的是洗去FeCl3、HCl等无机物.节省碱的用量,降低成本.
②10%NaOH溶液碱洗时发生氧化还原反应的化学反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O.
(6)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸汽,请在图2中画出,并标明所用试剂.
(7)工业生产中苯的流失情况如表所示:
| 项目 | 二氯苯 | 氯化尾气 | 蒸气 | 成品 | 不确定苯耗 | 合计 |
| 苯流失量(t/kg) | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.