题目内容
下列关于原电池的叙述中正确的是( )
| A、在锌、铜、CuSO4溶液组成的原电池中,负极质量减轻,正极质量增加 |
| B、在铁、铝、稀硫酸组成的原电池中,电子由铁片通过导线流向铝片 |
| C、在锌、铜、稀硫酸组成的原电池中,当电池工作时,硫酸根离子向正极移动 |
| D、在镁、铝、稀NaOH溶液组成的原电池中,镁是负极,铝是正极 |
考点:原电池和电解池的工作原理
专题:
分析:A、锌、铜、CuSO4溶液组成的原电池中,负极失电子,正极上阳离子得电子;
B、电子从负极流向正极;
C.原电池中阴离子向负极移动;
D、失电子的一极为负极.
B、电子从负极流向正极;
C.原电池中阴离子向负极移动;
D、失电子的一极为负极.
解答:
解:A、锌、铜、CuSO4溶液组成的原电池中,负极Zn失电子逐渐溶解质量减轻,正极上铜离子得电子生成Cu,质量增加,故A正确;
B、电子从负极流向正极,所以在铁、铝、稀硫酸组成的原电池中,铝为负极,铁为正极,则电子由铝片通过导线流向铁片,故B错误;
C、原电池中阴离子向负极移动,在锌、铜、稀硫酸组成的原电池中,所以硫酸根离子向负极移动,故C错误;
D、失电子的一极为负极,在镁、铝、稀NaOH溶液组成的原电池中,Al失电子为负极,故D错误;
故选A.
B、电子从负极流向正极,所以在铁、铝、稀硫酸组成的原电池中,铝为负极,铁为正极,则电子由铝片通过导线流向铁片,故B错误;
C、原电池中阴离子向负极移动,在锌、铜、稀硫酸组成的原电池中,所以硫酸根离子向负极移动,故C错误;
D、失电子的一极为负极,在镁、铝、稀NaOH溶液组成的原电池中,Al失电子为负极,故D错误;
故选A.
点评:本题考查原电池知识,侧重于原电池的组成、电极以及工作原理的考查,题目难度不大,注意相关基础知识的理解.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
下列关于营养物质的说法正确的是( )
| A、油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物 |
| B、氨基酸和蛋白质分子中都含有氨基和羧基,二者均有两性 |
| C、淀粉溶液和稀硫酸共热后发生水解反应,冷却后加少量银氨溶液,水浴加热后会出现光亮的银镜 |
| D、鸡蛋白溶液中加入浓硝酸溶液,出现白色沉淀,加热,沉淀变黄色,该过程叫作蛋白质的变性 |
下列反应无论怎样调整反应物的用量都只能生成一种物质的是( )
| A、甲烷和氯气混合后光照发生反应 |
| B、乙烯与氯化氢的加成反应 |
| C、1,3-丁二烯与氢气发生反应 |
| D、乙炔和氯气的加成反应 |
下列各组离子在溶液中能大量共存的是( )
| A、Fe3+、Na+、SO32-、I- |
| B、H+、NO3-、SO42-、Fe2+ |
| C、Cu2+、Mg2+、SO42-、NO3- |
| D、NH4+、Ba2+、NO3-、OH- |
一定条件下,将A、B、C三种物质各1mol通入一个密闭容器中发生反应:2A+B?2C,达到化学反应限度时,B的物质的量可能是( )
| A、1.5mol | B、1mol |
| C、0.5mol | D、0 |
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、最简单气态氢化物的热稳定性:R>Q |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、原子半径:T>Q>R |
| D、R的最高价氧化物对应的水化物和它的氢化物反应不能生成盐 |
下列关于碱金属元素和卤素的说法中,错误的是( )
| A、随核电荷数的增加,碱金属元素和卤素的熔沸点都逐渐降低 |
| B、碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
| C、钾与水的反应比钠与水的反应更剧烈 |
| D、溴单质与H2的反应比碘单质与H2的反应更剧烈 |
下列说法中正确的是( )
| A、6.8g固体KHSO4与3.9g固体Na2O2中阴离子数目相同 |
| B、常温下铁、铜均不溶于浓硫酸,说明常温下铁、铜与浓硫酸均不反应 |
| C、离子化合物中只含离子键 |
| D、中子数为18的氯原子可表示为18Cl |
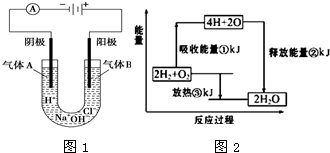 (1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化.已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收 249kJ的能量;形成水分子中1mol H-O键能够释放 463kJ能量.如图1表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上.
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化.已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收 249kJ的能量;形成水分子中1mol H-O键能够释放 463kJ能量.如图1表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上.