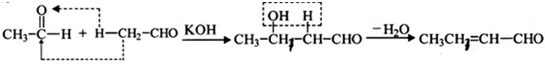题目内容
按要求回答问题:
(1)某元素原子最外层电子数是次外层的2倍,则该元素是 元素,其最高价氧化物的电子式是 .
(2)某元素的次外层电子数是最外层电子数的1/4,请写出该元素的核外电子排布式 .
(3)某元素原子核外M层电子数是L层电子数的一半,请写出该元素的价电子轨道表示式 .
(4)1~36号元素原子核外电子排布中未成对电子数最多的元素是 ,其基态原子的核外电子排布式 .
(5)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.其单质在一定条件下能与氧气反应,试写出该反应方程式 .
(1)某元素原子最外层电子数是次外层的2倍,则该元素是
(2)某元素的次外层电子数是最外层电子数的1/4,请写出该元素的核外电子排布式
(3)某元素原子核外M层电子数是L层电子数的一半,请写出该元素的价电子轨道表示式
(4)1~36号元素原子核外电子排布中未成对电子数最多的元素是
(5)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.其单质在一定条件下能与氧气反应,试写出该反应方程式
考点:原子结构与元素的性质
专题:原子组成与结构专题
分析:(1)某元素原子的最外层电子数是次外层电子数的两倍,则该元素原子有2个电子层,最外层电子数为4,为碳元素;
(2)元素原子次外层电子数是最外层电子数的
,原子只能有2个电子层,最外层电子数为8;
(3)某元素原子核外M层电子数是L层电子数的一半,则M层有4个电子,K、L层排满,所以原子核外共14电子;
(4)1~36号元素原子核外电子排布中未成对电子数最多的元素,故元素原子3d、4s均为半满;
(5)元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则其基态原子的电子排布式为1s22s22p63s23p63d104s1,则为Cu.
(2)元素原子次外层电子数是最外层电子数的
| 1 |
| 4 |
(3)某元素原子核外M层电子数是L层电子数的一半,则M层有4个电子,K、L层排满,所以原子核外共14电子;
(4)1~36号元素原子核外电子排布中未成对电子数最多的元素,故元素原子3d、4s均为半满;
(5)元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则其基态原子的电子排布式为1s22s22p63s23p63d104s1,则为Cu.
解答:
解:(1)某元素原子的最外层电子数是次外层电子数的两倍,则该元素原子有2个电子层,最外层电子数为4,为碳元素,其最高价氧化物是CO2,CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ;
;
故答案为:C; ;
;
(2)元素原子次外层电子数是最外层电子数的
,原子只能有2个电子层,最外层电子数为8,为O元素,其基态原子的电子排布式为:1s22s22p6,
故答案为:1s22s22p6;
(3)某元素原子核外M层电子数是L层电子数的一半,则M层有4个电子,K、L层排满,所以原子核外共14电子,则该元素为Si元素,其价电子轨道表示式为: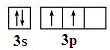 ,故答案为:
,故答案为: ;
;
(4)1~36号元素原子核外电子排布中未成对电子数最多的元素,故元素原子3d、4s均为半满,元素原子的价电子构型为3d54s1,则其基态原子的核外电子排布式[Ar]3d54s1,原子核外共24个电子,为Cr元素;
故答案为:Cr;[Ar]3d54s1;
(5)元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则其基态原子的电子排布式为1s22s22p63s23p63d104s1,则该元素为Cu,其单质在一定条件下与氧气反应方程式为:2Cu+O2
2CuO,
故答案为:2Cu+O2
2CuO.
 ;
;故答案为:C;
 ;
;(2)元素原子次外层电子数是最外层电子数的
| 1 |
| 4 |
故答案为:1s22s22p6;
(3)某元素原子核外M层电子数是L层电子数的一半,则M层有4个电子,K、L层排满,所以原子核外共14电子,则该元素为Si元素,其价电子轨道表示式为:
 ,故答案为:
,故答案为: ;
;(4)1~36号元素原子核外电子排布中未成对电子数最多的元素,故元素原子3d、4s均为半满,元素原子的价电子构型为3d54s1,则其基态原子的核外电子排布式[Ar]3d54s1,原子核外共24个电子,为Cr元素;
故答案为:Cr;[Ar]3d54s1;
(5)元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则其基态原子的电子排布式为1s22s22p63s23p63d104s1,则该元素为Cu,其单质在一定条件下与氧气反应方程式为:2Cu+O2
| ||
故答案为:2Cu+O2
| ||
点评:本题考查原子结构、核外电子排布、轨道式等,题目难度中等,侧重于对基础知识的考查,注意把握电子排布式的书写方法.

练习册系列答案
相关题目
有关如图装置的叙述不正确的是( )
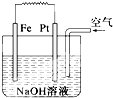

| A、这是电解NaOH溶液的装置 |
| B、该装置中Pt为正极,电极反应为O2+2H2O+4e-═4OH- |
| C、该装置中Fe为负极,电极反应为Fe-2e-═Fe2+ |
| D、这是一个原电池装置 |
物质的量之比为2:5的锌与稀硝酸恰好完全反应,若硝酸被还原的产物为NH4NO3,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
| A、1:4 | B、1:9 |
| C、2:3 | D、2:5 |
下列说法错误的是( )
| A、在水中的溶解度NH3>CH4 |
| B、晶体熔点的高低SiO2>CO2 |
| C、金属键的强弱Li>K |
| D、晶格能的大小NaF>MgO |
下列叙述中能确定A金属性一定比B金属性强的是( )
| A、A原子的最外层电子数比B原子的最外层电子数少 |
| B、A原子的电子层数比B原子的电子层数多 |
| C、1 mol A与足量酸反应生成的H2比1 mol B与足量酸反应生成的H2多 |
| D、常温时,A能从水中置换出氢,而B不能 |
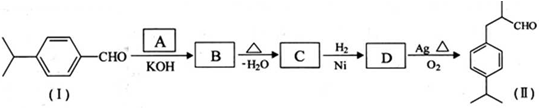
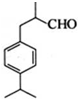 是一种重要的香料.用有机物I为原料可以合成兔耳草醛,其合成路线如图所示:
是一种重要的香料.用有机物I为原料可以合成兔耳草醛,其合成路线如图所示: