题目内容
6.在相同温度和压强条件下,质量相同的O2、NH3、H2、Cl2四种气体中,体积最大的是H2.分析 同温同压下气体摩尔体积相等,根据V=nVm=$\frac{m}{M}$Vm可知,气体的摩尔质量越大,该气体的体积越大,结合气体的摩尔质量大小进行解答.
解答 解:在相同温度和压强条件下具有相同的气体摩尔体积,根据V=nVm=$\frac{m}{M}$Vm可知,气体的摩尔质量越大,该气体的体积越大,
O2、NH3、H2、Cl2四种气体中摩尔质量大小关系为:Cl2>O2>NH3>H2,则气体体积最大的为H2,
故答案为:H2.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与气体摩尔体积的关系为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.关于2mol SO2的叙述中,正确的是( )
| A. | 体积为44.8L | B. | 含有4mol氧原子 | ||
| C. | 分子数为6.02×1023 | D. | 摩尔质量为128g |
11.油脂皂化后,使肥皂和甘油从混合物里充分分离,可以采用( )
①分液 ②蒸馏 ③过滤 ④盐析 ⑤渗析.
①分液 ②蒸馏 ③过滤 ④盐析 ⑤渗析.
| A. | ①② | B. | ③④ | C. | ②③④ | D. | ②③⑤ |
18.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol•L-1NaClO溶液中:Na+、K+、I-、NO3- | |
| B. | 0.1 mol•L-1氨水溶液:K+、Na+、NO3-、Al3+ | |
| C. | 0.1 mol•L-1Na2CO3溶液中:NH4+、K+、SO42-、Cl- | |
| D. | c(H+)/c(OH-)=1×1012的溶液中:Ca2+、Na+、SiO32-、C6H5O- |
15.如图为冰晶体的结构模型,大球代表O原子,小球代表H原子.下列有关说法正确的是( )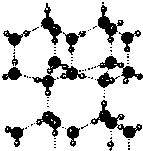

| A. | 冰晶体中每个水分子与另外四个水分子形成四面体 | |
| B. | 冰晶体具有空间网状结构,是原子晶体 | |
| C. | 水分子间通过H-O键形成冰晶体 | |
| D. | 冰晶体熔化时,H-O键断裂 |
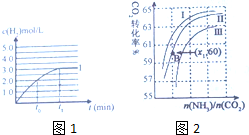 氨气是一种重要的化工产品,在生产和科研中应用广泛,氨气是工业合成氨的原料之一,工业上制取氨气有下列两种途径:
氨气是一种重要的化工产品,在生产和科研中应用广泛,氨气是工业合成氨的原料之一,工业上制取氨气有下列两种途径: 氨是重要的化工原料,用途广泛.
氨是重要的化工原料,用途广泛.