题目内容
19. 室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的
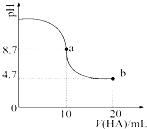
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
| A. | a点所示溶液中c(HA)>c(A-) | |
| B. | a点所示溶液中c(Na+)=c(A-)+c(HA) | |
| C. | 当加入HA溶液10ml时,$\frac{{K}_{w}}{c({H}^{+})}$<1.0×10-7mol•L-1 | |
| D. | b点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) |
分析 A.a点加入10mLHA溶液,溶质为NaA,A-的水解程度减小,则c(HA)<c(A-);
B.a点溶质为NaA溶液,根据物料守恒判断;
C.$\frac{{K}_{w}}{c({H}^{+})}$=c(OH-),根据a点溶液的pH计算;
D.b点溶质为等浓度的NaA和HA,HA的电离程度较小,则c(HA)>c(H+).
解答 解:A.a点时氢氧化钠与HA恰好反应生成NaA,由于A-的水解程度减小,则c(HA)<c(A-),故A错误;
B.a点所示溶液中溶质为NaA,根据物料守恒可得:c(Na+)=c(A-)+c(HA),故B正确;
C.当加入HA溶液10mL时,$\frac{{K}_{w}}{c({H}^{+})}$=$\frac{1×1{0}^{-14}}{1×1{0}^{-8.7}}$mol/L=1.0×10-5.3mol•L-1>1.0×10-7mol•L-1,故C错误;
D.b点加入20mLHA溶液,反应后溶质为等浓度的NaA和HA,HA的电离程度较小,则c(HA)>c(H+),正确的离子浓度大小为:c(Na+)>c(A-)>c(HA)>c(H+),故D错误;
故选B.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
3.2015年我国药物化学家屠呦呦因发明抗疟疾新药青蒿素和双氢青蒿素被授予诺贝尔生理学或医学奖.以异胡薄荷醇为起始原料是人工合成青蒿素的途径之一(如图).下列说法正确的是( )


| A. | 异胡薄荷醇遇FeCl3溶液显紫色 | |
| B. | 每个青蒿素分子中含有4个六元环 | |
| C. | 异胡薄荷醇可发生消去反应、加成反应 | |
| D. | 青蒿素在热的酸、碱溶液中均可稳定存在 |
7.把mg铜丝灼烧变黑,立即放入下列物质中,能使铜丝变红但质量减小的是( )
| A. | NaOH溶液 | B. | CH3COOH | C. | 水 | D. | CH3CH2OH |
14.在Na2O2与CO2的反应中,被氧化元素与被还原元素的质量比是( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 8:53 |
11.下列关于物质性质的叙述中,正确的是( )
| A. | 硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性 | |
| B. | N2是大气中的主要成分之一,雷雨时,可直接转化为NO2 | |
| C. | Cl2能与金属活动顺序表中大多数金属反应 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质活泼 |
9.在蒸发发皿中加热蒸干并灼烧(低于400℃)下列的溶液,可以得到该物质的固体是( )
| A. | 氯化铝溶液 | B. | 硫酸亚铁溶液 | C. | 碳酸氢钠溶液 | D. | 硫酸铝溶液 |
 已知X、Y是两种性质相似的短周期元素.
已知X、Y是两种性质相似的短周期元素. ,它们的单质都必须采用电解法制备,但都无需密封保存,
,它们的单质都必须采用电解法制备,但都无需密封保存, .(2)Y元素在周期表中位置第三周期ⅢA族.
.(2)Y元素在周期表中位置第三周期ⅢA族.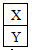 ,X是形成化合物种类最多的元素.
,X是形成化合物种类最多的元素.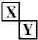 ,X、Y的最高价含氧酸的浓溶液都有强氧化性.
,X、Y的最高价含氧酸的浓溶液都有强氧化性.