题目内容
已知X是一种正盐,它既能与强酸反应,又能与强碱反应;A为共价化合物,甲为黑色固体,B为红色固体;E常用于铜制电路板的腐蚀;F为单质,其构成的原子的核外电子排布第5层上有7个电子;溶液中的水以及部分反应物或生成物未标出.

(1)写出X的化学式 .
(2)化合物丙与A组成元素相同,1mol丙含12mol电子,请写出丙的电子式: .

(1)写出X的化学式
(2)化合物丙与A组成元素相同,1mol丙含12mol电子,请写出丙的电子式:
考点:无机物的推断
专题:
分析:X是一种正盐,它既能与强酸反应,又能与强碱反应,说明X为弱酸弱碱盐,X与氢氧化钠反应,应为X中的弱碱阳离子与氢氧根离子的反应,生成A为共价化合物,可确定A为NH3,甲为黑色固体,B为红色固体,则甲为氧化铜,B为铜;E常用于铜制电路板的腐蚀,则E为氯化铁溶液;F为单质,其构成的原子的核外电子排布第5层上有7个电子,则F为碘,根据题中各物质转化关系,X与乙反应生成C,乙应为酸,C能被氧气氧化,且与氯化铁能再反应,则可推知C为硫化氢,D为二氧化硫,二氧化硫和碘反应生成乙为硫酸,X与硫酸反应生成硫化氢,则X为硫化铵,氯化铁与二氧化硫也能反应生成硫酸和H为氯化亚铁,铜与浓硫酸加热生成Y为硫酸铜,电解硫酸铜溶液得铜和硫酸以及氧气,符合各物质的转化关系,据此答题.
解答:
解:X是一种正盐,它既能与强酸反应,又能与强碱反应,说明X为弱酸弱碱盐,X与氢氧化钠反应,应为X中的弱碱阳离子与氢氧根离子的反应,生成A为共价化合物,可确定A为NH3,甲为黑色固体,B为红色固体,则甲为氧化铜,B为铜;E常用于铜制电路板的腐蚀,则E为氯化铁溶液;F为单质,其构成的原子的核外电子排布第5层上有7个电子,则F为碘,根据题中各物质转化关系,X与乙反应生成C,乙应为酸,C能被氧气氧化,且与氯化铁能再反应,则可推知C为硫化氢,D为二氧化硫,二氧化硫和碘反应生成乙为硫酸,X与硫酸反应生成硫化氢,则X为硫化铵,氯化铁与二氧化硫也能反应生成硫酸和H为氯化亚铁,铜与浓硫酸加热生成Y为硫酸铜,电解硫酸铜溶液得铜和硫酸以及氧气,符合各物质的转化关系,
(1)根据上面的分析可知,X为硫化铵,化学式为(NH4)2S,故答案为:(NH4)2S;
(2)A为NH3,化合物丙与A组成元素相同,1mol丙含12mol电子,则丙为NH4H,它的电子式为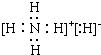 ,故答案为:
,故答案为: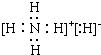 .
.
(1)根据上面的分析可知,X为硫化铵,化学式为(NH4)2S,故答案为:(NH4)2S;
(2)A为NH3,化合物丙与A组成元素相同,1mol丙含12mol电子,则丙为NH4H,它的电子式为
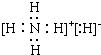 ,故答案为:
,故答案为: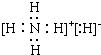 .
.
点评:本题考查无机物推断,题目难度中等,根据物质的颜色以及用途、结构等结合物质的转化关系,进行综合推断是解题的关键,答题时要熟练运用元素化合物知识.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
已知:①C(s)、H2(g)的燃烧热分别是393.5kJ?mol-1 、285.8kJ?mol-1
②CH3COOH(l)+2O2 (g)═2CO2 (g)+2H2O (g)△H1=-782.3kJ?mol-1
③H2O(l)═H2O (g)△H2=+44.0kJ?mol-1 .
则反应:2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热△H为( )
②CH3COOH(l)+2O2 (g)═2CO2 (g)+2H2O (g)△H1=-782.3kJ?mol-1
③H2O(l)═H2O (g)△H2=+44.0kJ?mol-1 .
则反应:2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热△H为( )
| A、-576.3kJ?mol-1 |
| B、-532.3kJ?mol-1 |
| C、-488.3kJ?mol-1 |
| D、-244.15kJ?mol-1 |
用石墨电极,电解一定浓度的下列四种物质的水溶液.电解一段时间后,若只往所得溶液中适量的水,可以恢复到电解前的状态.该物质是( )
| A、AgNO3 |
| B、NaCl |
| C、KOH |
| D、CuCl2 |
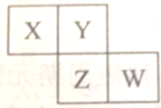 XYZW均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的
XYZW均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的| 7 |
| 10 |
| A、阴离子的半径从大到小的排列顺序为X>Y>Z>W |
| B、X元素的氢化物分子间可形成氢键 |
| C、Y的两种同素异形体在一定条件下可以相互转化 |
| D、最高价氧化物对应的水化物的酸性:W>Z |
 超细碳酸钙,粒径范围为1-100nm,其应用非常广泛.下图为某化工企业生产超细碳酸钙的原理
超细碳酸钙,粒径范围为1-100nm,其应用非常广泛.下图为某化工企业生产超细碳酸钙的原理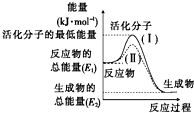 在化学反应中,只有活化分子的有效碰撞才能引起化学反应.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察右图,然后回答下列问题:
在化学反应中,只有活化分子的有效碰撞才能引起化学反应.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察右图,然后回答下列问题: