题目内容
14.除去物质中含少量杂质的方法错误是( )| 选项 | 物质(括号内为杂质) | 实验方法 |
| A | K2SO4 (K2CO3) | 加入稀硫酸使溶液呈中性 |
| B | NaCl (KNO3) | 样品配制成热饱和溶液,冷却结晶,过滤 |
| C | CO2(HCl) | 通过NaHCO3饱和溶液,干燥 |
| D | 溴苯(溴) | 加入足量NaOH溶液,充分振荡,分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.K2CO3与硫酸反应生成硫酸钾;
B.NaCl的量多,硝酸钾少,应蒸发结晶;
C.HCl与饱和碳酸氢钠溶液反应生成二氧化碳;
D.溴与NaOH反应后,与溴苯分层.
解答 解:A.K2CO3与硫酸反应生成硫酸钾,则加入稀硫酸使溶液呈中性可除杂,故A正确;
B.NaCl的量多,硝酸钾少,应蒸发结晶,不能冷却结晶分离,故B错误;
C.HCl与饱和碳酸氢钠溶液反应生成二氧化碳,则通过NaHCO3饱和溶液,干燥可除杂,故C正确;
D.溴与NaOH反应后,与溴苯分层,然后分液可分离,故D正确;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
4.下列叙述正确的是( )
| A. | 强电解质都是离子化合物,弱电解质都是共价化合物 | |
| B. | 强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子 | |
| C. | 向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体 | |
| D. | 向Na2CO3饱和溶液中,通入过量的CO2后,加热蒸干得NaHCO3晶体 |
5.某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g)$→_{△}^{催化剂}$2SO3(g);△H<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( )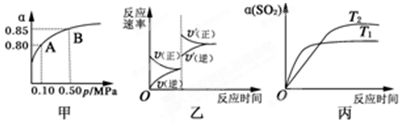

| A. | 由图甲推断,B点SO2的平衡浓度为0.3 mol•L-1 | |
| B. | 由图甲推断,A点对应温度下该反应的平衡常数为800(L•mol-1) | |
| C. | 达平衡后,若增大容器容积,则反应速率变化图象可以用图乙表示 | |
| D. | 压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
9.有机物命名正确的是( )
| A. | CH2BrCH2Br 二溴乙烷 | B. | CH3OOCCH3甲酸乙酯 | ||
| C. | 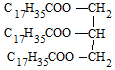 硬脂酸甘油脂 硬脂酸甘油脂 | D. | 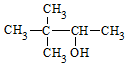 3,3-二甲基-2-丁醇 3,3-二甲基-2-丁醇 |
3.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②天然气和水煤气都是可再生能源;③冰和干冰均既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋均既是化合物又是酸;⑥纯碱和熟石灰都是碱.上述说法正确的是( )
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ③⑤⑥ | D. | ①③④ |
10.在相同压强下,经过相同反应时间测得如下实验数据:
【备注】甲醇选择性:转化的CO2中生成甲醇的百分比.
(1)测得实验数据时,反应不是(填“是”或“不是”)处于平衡状态.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有CD
A.使用催化剂A B.使用催化剂B C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明:在相同温度下,因为催化剂A和B对反应Ⅰ的催化能力不同,所以在该时刻不同的催化剂对CO2转化成CH3OH的选择性有显著的影响.
| 实验编号 | T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 1 | 543 | 催化剂A | 12.3 | 42.3 |
| 2 | 543 | 催化剂B | 10.9 | 72.7 |
| 3 | 553 | 催化剂A | 15.3 | 39.1 |
| 4 | 553 | 催化剂B | 12.0 | 71.6 |
(1)测得实验数据时,反应不是(填“是”或“不是”)处于平衡状态.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有CD
A.使用催化剂A B.使用催化剂B C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明:在相同温度下,因为催化剂A和B对反应Ⅰ的催化能力不同,所以在该时刻不同的催化剂对CO2转化成CH3OH的选择性有显著的影响.
8.pC类似pH,是指稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol•L-1,则该溶液中溶质的pC=3.下列叙述正确的是( )
| A. | 常温下,0.01mol•L-1的醋酸溶液中,pC(H+)=2 | |
| B. | 常温下,向0.01mol•L-1的氨水中加入等体积等浓度的盐酸,混合液的pC(H+)<7 | |
| C. | 100℃时,0.01mol•L-1的NaOH溶液中,pC(OH-)+pC(H+)=14 | |
| D. | 100℃时,CaCO3的Ksp=2.5×10-9,其饱和溶液中pC(Ca2+)+pC(CO32-)=9 |