题目内容
9.氮的氧化物(如NO2、NO4、N2O5等)应用很广,在一定条件下可以相互转化.(l)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.
己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)?N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H=△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4.
(2)从N2O5在一定条件下发生分解:2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/mol/L | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
1.00~3.00min内,O2的平均反应速率为0.090mol•L-1•min-1.
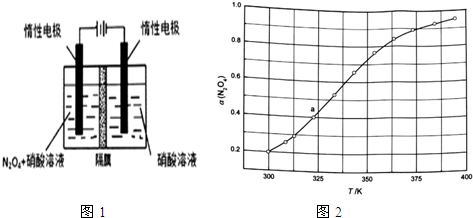
(3)从N2O4与NO2之间存在反应N2O4?2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=115.2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)?2NO2(g)是吸热反应还是放热反应,说明理由吸热反应,温度升高,α(N2O4)增加,说明平衡右移,若要提高N2O4转化率,除改变反应温度外,其他措施有减小体系压强、移出NO2(要求写出两条).
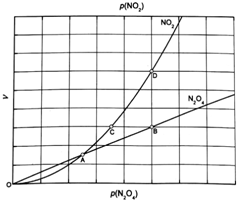
③对于反应N2O4(g)?2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2[p(NO2)]2.其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl=$\frac{1}{2}$K2.Kp,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由B点与D点,满足平衡条件υ(NO2)=2υ(N2O4).
分析 (1)由N2O4制取N2O5需要失去电子,所以N2O5在阳极区生成,N2O4在阳极发生氧化反应失去电子生成N2O5;
①2NO(g)+O2(g)═2NO2(g)△H1
②NO(g)+O3(g)═NO2(g)+O2(g)△H2
③2NO2(g)?N2O4(g)△H3
④2N2O5(g)═4NO2(g)+O2(g)△H4
将方程式②-$\frac{1}{2}$①-③-$\frac{1}{2}$④得N2O4(g)+O3(g)═N2O5(g)+O2(g),焓变进行相应的改变;
(2)相同条件下,气体的物质的量之比等于其压强之比;
2N2O5(g)═4NO2(g)+O2(g)
开始(mol/L)1.00 0 0
反应(mol/L)0.50 1.00 0.25
2min(mol/L)0.50 1.00 0.25
反应前后气体的压强之比等于其物质的量之比;
先计算五氧化二氮的反应速率,再根据同一时间段内各物质的反应速率之比等于其计量数之比计算氧气反应速率;
(3)①化学平衡常数K=$\frac{生成物分压幂之积}{反应物分压幂之积}$;
②升高温度平衡向吸热方向移动;减小体系压强、移出NO2都使平衡正向移动;
③化学平衡常数Kp=[p(NO2)]2÷p(N2O4),二者的反应速率之比等于其计量数之比;
满足平衡条件υ(NO2)=2υ(N2O4)即为平衡点.
解答 解:(1)从电解原理来看,N2O4制备N2O5为氧化反应,则N2O5应在阳极区生成,反应式为N2O4+2HNO3-2e-═2N2O5+2H+,
①2NO(g)+O2(g)═2NO2(g)△H1
②NO(g)+O3(g)═NO2(g)+O2(g)△H2
③2NO2(g)?N2O4(g)△H3
④2N2O5(g)═4NO2(g)+O2(g)△H4
将方程式②-$\frac{1}{2}$①-③-$\frac{1}{2}$④得N2O4(g)+O3(g)═N2O5(g)+O2(g),得N2O4(g)+O3(g)═N2O5(g)+O2(g),
则该反应△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4,
故答案为:N2O4+2HNO3-2e-═2N2O5+2H+;△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4;
(2)相同条件下,气体的物质的量之比等于其压强之比;
2N2O5(g)═4NO2(g)+O2(g)
开始(mol/L)1.00 0 0
反应(mol/L)0.50 1.00 0.25
2min(mol/L)0.50 1.00 0.25
反应前后气体的压强之比等于其物质的量之比,所以p:p0=(0.50+1.00+0.25)mol:1.00mol=1.75;
v(N2O5)=$\frac{0.71-0.35}{2}$mol/(L.min)=0.18mol/(L.min),再根据同一时间段内各物质的反应速率之比等于其计量数之比得氧气反应速率为0.090 mol•L-1•min-1,
故答案为:1.75;0.090 mol•L-1•min-1;
(3)①四氧化二氮的转化率是0.4,设原来四氧化二的物质的量为xmol,转化的物质的量为0.8xmol,则混合气体的物质的量=(x-0.4x+0.8x)mol=1.4xmol,相同条件下,气体的压强之比等于其物质的量之比,所以反应后压强=$\frac{108KPa}{xmol}×1.4xmol$=151.2KPa,
四氧化二氮的分压=151.2KPa×$\frac{0.6xmol}{1.4xmol}$=64.8KPa,
二氧化氮的分压=151.2KPa×$\frac{0.8xmol}{1.4xmol}$=86.4KPa,
化学平衡常数K=$\frac{生成物分压幂之积}{反应物分压幂之积}$=$\frac{86.{4}^{2}}{64.8}$=115.2,
故答案为:115.2;
②根据图知,升高温度转化率增大,升高温度平衡向吸热方向移动,则正反应是吸热反应,若要提高N2O4转化率,除改变反应温度外,其他措施有减小体系压强、移出NO2,
故答案为:吸热反应;温度升高,α(N2O4)增加,说明平衡右移;减小体系压强、移出NO2;
③化学平衡常数Kp=[p(NO2)]2÷p(N2O4),二者的反应速率之比等于其计量数之比,
所以υ(NO2):υ(N2O4)=k2[p(NO2)]2:k1•p(N2O4)=2:1,
化学平衡常数Kp=[p(NO2)]2÷p(N2O4),
则K1=$\frac{1}{2}$K2.Kp,
满足平衡条件υ(NO2)=2υ(N2O4)即为平衡点,BD点的压强之比等于其反应速率之比为1:2,所以BD为平衡点,
故答案为:$\frac{1}{2}$K2.Kp;B点与D点,满足平衡条件υ(NO2)=2υ(N2O4).
点评 本题考查化学平衡有关计算,为高频考点,涉及平衡计算、盖斯定律等知识点,侧重考查学生分析计算及获取信息解答问题能力,难点是(3)题平衡常数的计算,注意分压的计算方法,题目难度中等.

H2(g)+Br2(g)?2HBr(g)已知加入1molH2和2molBr2时,达到平衡后,生成a molHBr,(见下表“已知项”).在相同的条件下,改变起始加入情况,填写表中空白:
| 编号 | 起始状态 | 平衡时HBr物质的量(mol) | ||
| H2 | Br2 | HBr | ||
| 已知 | 1 | 2 | 0 | a |
| (1) | 2 | 4 | 0 | 2a |
| (2) | 0 | 0.5 | 1 | 0.5a |
| 装置 | 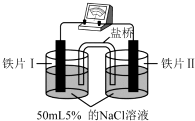 | 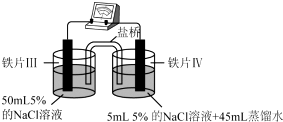 |
| 现象 | 电流计指针未发生偏转 | 电流计指针偏转 |
| A. | “电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 | |
| B. | 用K3[Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极 | |
| C. | 铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,二者的腐蚀速率相等 | |
| D. | 铁片Ⅳ的电极反应式为Fe-3e-=Fe3+ |
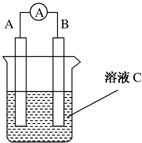 如图所示是原电池的装置图(
如图所示是原电池的装置图( 为电流表).请回答:
为电流表).请回答: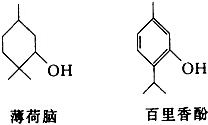 下列物质是几种常见香精的主要成分:
下列物质是几种常见香精的主要成分: .
.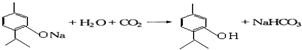 .
.