题目内容
14.用NA表示阿伏加德罗常数的值.下列说法正确的是( )| A. | 常温常压下,2.24 L H2O中分子的数目为0.1 NA | |
| B. | 0.1 mol•L-1 NH4Cl溶液中含有Cl-的数目为0.1 NA | |
| C. | 常温下,1.7 g NH3中含有原子数目为0.3 NA | |
| D. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA |
分析 A、标况下水为液体;
B、溶液体积不明确;
C、求出氨气的物质的量,然后根据氨气中含4个原子来分析;
D、氧气和臭氧均由氧原子构成.
解答 解:A、标况下水为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、溶液体积不明确,故溶液中的氯离子的个数无法计算,故B错误;
C、1.7g氨气的物质的量为0.1mol,而氨气中含4个原子,故0.1mol氨气中含0.4NA个原子,故C错误;
D、氧气和臭氧均由氧原子构成,故32g氧气和臭氧的混合物中含有的氧原子的物质的量为2mol,个数为2NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
相关题目
5.利用下列实验装置进行实验,不能达到实验目的是( )
| A. |  用四氯化碳提取溴水中的溴单质 | B. |  用自来水制取蒸馏水 | ||
| C. | 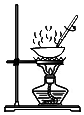 碘水中提取碘 | D. | 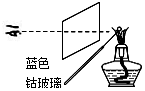 检验溶液中的K+ |
2.将三份1mol X气体和3mol Y气体分别充入体积为2L的A,B,C三个容器中,发生反应X(g)+3Y(g)?2Z(g).2min后反应达到平衡,测得A中剩余0.4mol X,B中Y的平衡浓度为0.5mol/L,C中用Z表示的反应速率为:v(Z)=0.3mol/(L•min),则这段时间内三个容器中反应速率的大小关系为( )
| A. | B>A>C | B. | A>B=C | C. | B>A=C | D. | B>C>A |
9.下列解释事实的离子方程式正确的是( )
| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H ++NO 3-═Fe 3++NO↑+2H 2O | |
| B. | 向Ca(ClO) 2溶液中通入过量CO 2制取次氯酸:2ClO-+H 2O+CO 2═2HClO+CO 32- | |
| C. | 向酸性KMnO 4溶液中通入SO 2:2MnO 4-+5SO 2+4OH -═2Mn 2++5SO 42-+2H 2O | |
| D. | 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ |
6.下列各组中两溶液间的反应,不能用同一离子方程式来表示的是( )
| A. | Na2CO3+HCl; K2CO3+HNO3 | B. | Fe+HCl;Fe+H2SO4 | ||
| C. | BaCl2+Na2SO4;Ba(OH)2+H2SO4 | D. | NaOH+H2O;Ba(OH)2+HCl |
3.下列物质的颜色按“红、橙、黄、绿、蓝、紫”顺序排列的是( )
①CuSO4•5H2O ②S ③溴水 ④FeCl2溶液⑤KMnO4溶液 ⑥硫氰化铁溶液.
①CuSO4•5H2O ②S ③溴水 ④FeCl2溶液⑤KMnO4溶液 ⑥硫氰化铁溶液.
| A. | ⑥③①②④⑤ | B. | ⑤④③①②⑥ | C. | ⑥③②④①⑤ | D. | ②③①④⑤⑥ |
4.下列有关物质用途的说法,正确的是( )
| A. | 四氧化三铁俗称铁红,可用于作油漆、红色涂料 | |
| B. | 石英可用于制电脑芯片 | |
| C. | 纯碱可用于治疗胃酸过多 | |
| D. | 过氧化钠可用作于潜艇的供氧剂 |
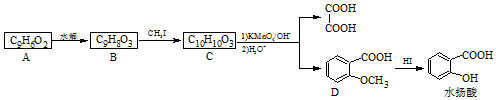

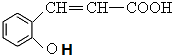 +CH3I→
+CH3I→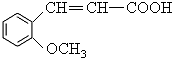 +HI,该反应类型为取代反应,该反应步骤的目的是保护酚羟基,使之不被氧化.
+HI,该反应类型为取代反应,该反应步骤的目的是保护酚羟基,使之不被氧化.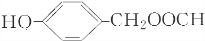 或
或 .
.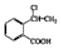 合成
合成 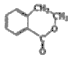 (用反应流程图表示,并注明反应条件).
(用反应流程图表示,并注明反应条件).
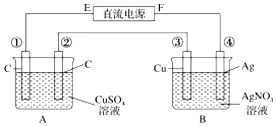 如图所示,通电5min后,第③极增重2.16g,此时CuSO4恰好电解完.设A池中原混合溶液的体积为200mL.
如图所示,通电5min后,第③极增重2.16g,此时CuSO4恰好电解完.设A池中原混合溶液的体积为200mL.