题目内容
19.在某酸性溶液中,能大量共存的离子组是( )| A. | Fe2+、K+、C1-、NO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、AlO2- | D. | Ba2+、K+、SO42-、C1- |
分析 强酸溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不能相互促进水解等,则离子大量共存,以此来解答.
解答 解:A.酸性条件下,Fe2+、NO3-发生氧化还原反应而不能大量共存,故A错误;
B.酸溶液中该组离子之间不反应,可大量共存,故B正确;
C.酸溶液中不能大量存在AlO2-,故C错误;
D.Ba2+、SO42-反应生成沉淀而不能大量共存,故D错误.
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.在2L的恒容容器中,充入1molA和3molB,并在一定条件下发生如下反应:A(g)+3B(g)?2C(g);经3s后达到平衡,测得C气体的浓度为0.6mol•L-1,下列说法中不正确的是( )
| A. | 用A表示反应的速率为0.1 mol•L-1•s-1 | |
| B. | 用B表示反应速率为0.4 mol•L-1•s-1 | |
| C. | 3s时生成C的物质的量为1.2mol | |
| D. | 3s时B的浓度为0.6mol•L-1 |
10.设阿伏伽德罗常数为NA,下列有关说法正确的是( )
| A. | 常温常压下,8g O2中电子数为4NA | |
| B. | 3.4gNH3中含原子总数为0.6 NA | |
| C. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量约为28g | |
| D. | 标况下,33.6 L的四氯化碳中,四氯化碳分子数为1.5NA |
7.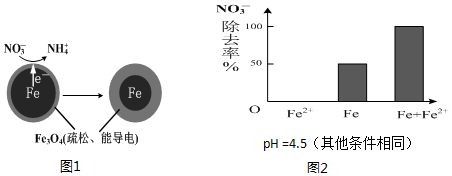 用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.
用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.
(1)Fe还原水体中NO3-的反应原理如图1所示.正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如表:
pH=4.5时,NO3-的去除率低.其原因是FeO(OH)不导电,阻碍电子转移.
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:pH=4.5(其他条件相同)
Ⅰ.Fe2+直接还原NO3-;Ⅱ.Fe2+破坏FeO(OH)氧化层.
①对比实验,结果如图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.
 用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.
用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.(1)Fe还原水体中NO3-的反应原理如图1所示.正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如表:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 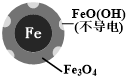 | 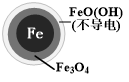 |
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:pH=4.5(其他条件相同)
Ⅰ.Fe2+直接还原NO3-;Ⅱ.Fe2+破坏FeO(OH)氧化层.
①对比实验,结果如图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.
14.某溶液中,滴加KSCN溶液时无明显现象发生,再滴入少量氯水,溶液立即显红色.则原溶液中可能含有( )
| A. | Na+ NH4+ Cl- | B. | Fe3+Fe2+SO42- | ||
| C. | K+Fe3+NO3- | D. | Na+Fe2+ Cl- |
11.下列关于Na2CO3和NaHCO3的说法不正确的是( )
| A. | 受热时的稳定性:Na2CO3>NaHCO3 | |
| B. | 使酚酞试液变红的程度:Na2CO3>NaHCO3 | |
| C. | 与同浓度同体积HCl反应产生气泡的速率:Na2CO3<NaHCO3 | |
| D. | 同物质的量与足量HCl反应生成CO2的量:Na2CO3<NaHCO3 |
1.向100mL0.04mol/L的Ca(OH)2溶液中通入CO2气体,当得到0.1g沉淀时,通入CO2的物质的量是( )
| A. | 0.014 mol | B. | 0.01 mol | C. | 0.007 mol | D. | 0.005 mol |
2.下列药品的保存错误的是( )
| A. | 白磷放在水中 | |
| B. | 酒精等易燃物应敞口放置且远离火源 | |
| C. | 氯酸钾、硝酸铵不要同可燃物混放,防爆炸 | |
| D. | 浓硫酸与固体氢氧化钠都需要密封保存 |