题目内容
4.三氯化磷分子的空间构型是三角锥形而不是平面正三角形.下列关于PCl3分子空间构型理由的叙述,正确的是( )| A. | PCl3分子中三个共价键的键能、键长、键角均相等 | |
| B. | PCl3分子中的P-Cl键都是p-p σ键 | |
| C. | PCl3分子中三个P-Cl键的键长相等,键角为100.1° | |
| D. | PCl3分子中三个P-Cl键都是极性共价键 |
分析 分子的空间构型是平面正三角形,则其键角应该为120°,根据分子的键角分析.
解答 解:PCl3分子中P原子价层电子对数为4,采用sp3杂化,含有1个孤电子对,分子的空间构型是三角锥形,三角锥形分子的键角小于平面正三角形的键角,平面正三角形,则其键角应该为120°,已知PCl3分子中P-Cl键的三个键角都是100.1°,所以三氯化磷分子的空间构型是三角锥形而不是平面正三角形,
故选C.
点评 本题考查了分子的空间构型与键角的判断,题目难度不大,注意平面正三角形分子的键角为120°.

练习册系列答案
相关题目
13.下列防止钢铁锈蚀的措施不合理的是 ( )
| A. | 在自行车的钢圈表面镀镍 | B. | 在地下钢铁管道上连接铜块 | ||
| C. | 改变金属内部结构制成不锈钢 | D. | 健身器村刷油漆或包上一层塑料层 |
15.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A. | 1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 | |
| B. | 0.1 L 3 mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5gSiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
12.短周期元素X和Y可以形成XY4型化合物,若X的原子序数为m,Y的原子序数为n,则m和n的相互关系为( )
| A. | m+13=n | B. | n+5=m | C. | m+8=n | D. | n+11=m |
19.下列物质的水溶液因水解而呈酸性的是( )
| A. | NaOH | B. | (NH4)2SO4 | C. | Na2CO3 | D. | NaCl |
9.下列离子方程式正确的是( )
| A. | 金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的NaOH溶液 Al3++3OH-═Al(OH)3↓ | |
| C. | Fe3O4与稀硝酸溶液反应:2Fe3O4+18H+═6Fe3++H2↑+8H2O | |
| D. | NaHSO4溶液与足量Ba(OH)2溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
13.有硫酸铁溶液80g,它的密度是dg/cm3,含有2.8gFe3+,则有关该溶液的说法不正确的是( )
| A. | 溶质的质量分数是12.5% | |
| B. | 溶液的物质的量浓度是5d/16mol/L | |
| C. | Fe3+的物质的量浓度是5d/8mol/L | |
| D. | 硫酸根离子的物质的量浓度是10d/16mol/L |
14.下列有关电解质溶液的叙述正确的是( )
| A. | 升高温度时,HF的Ka增大,水的Kw不变 | |
| B. | 向Mg(OH)2悬浊液中加入NH4Cl固体,c(Mg2+)、c(OH-)浓度均增大 | |
| C. | 常温下,0.lmol/LNH4Cl 溶液的 pH>7 | |
| D. | 0.1mol/LNa2SO3溶液中,加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
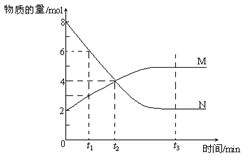 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,反应的化学方程式为2N?M.
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,反应的化学方程式为2N?M.