题目内容
9.下列有关元素周期律的叙述中,正确的是( )| A. | 氧化性强弱:F2<Cl2 | B. | 金属性强弱:Al<Na | ||
| C. | 酸性强弱:H2CO3<HNO3 | D. | 碱性强弱:NaOH<Mg(OH)2 |
分析 A.非金属性越强,对应单质的氧化性越强;
B.同周期从左向右金属性减弱;
C.非金属性越强,对应最高价含氧酸的酸性越强;
D.金属性越强,对应碱的碱性越强.
解答 解:A.非金属性越强,对应单质的氧化性越强,则氧化性强弱:F2>Cl2,故A错误;
B.同周期从左向右金属性减弱,则金属性强弱:Al<Na,故B正确;
C.非金属性越强,对应最高价含氧酸的酸性越强,则酸性强弱:H2CO3<HNO3,故C正确;
D.金属性越强,对应碱的碱性越强,则碱性强弱:NaOH>Mg(OH)2,故D错误;
故选BC.
点评 本题考查元素的性质及元素周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
20.如图纵坐标为反应物的转化率,横坐标为温度(t℃),下列符合此图情况的反应是( )
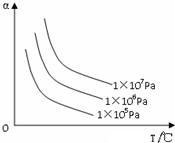

| A. | C(s)+CO2(g)?2CO(g);△H>0 | B. | H2(g)+Br2(g)?2HBr(g);△H<0 | ||
| C. | N2(g)+3H2(g)?2NH3(g);△H<0 | D. | 2SO3(g)?2SO2(g)+O2(g);△H>0 |
17.对于平衡体系:aA(g)+bB(g)?cC(g)+dD(g);正反应放热,有下列判断,其中正确的是( )
| A. | 若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.48倍,则a+b大于c+d | |
| B. | 若反应开始容器中只有A和B,平衡时,A、B的转化率相等,则A、B的物质的量之比为1:1 | |
| C. | 若平衡体系中共有气体xmol,再向其中充入bmolB,达到平衡时气体总物质的量为(x+b)mol,则a+b=c+d | |
| D. | 若a+b=c+d,升高温度时,A的体积分数不变 |
4.在容积固定的密闭容器中,对于反应2SO2(g)+O2(g)?2SO3(g)△H<0.下列判断正确的是( )
| A. | 增大反应体系的压强,平衡后SO2的浓度、转化率、体积分数都增加 | |
| B. | 当单位时间内消耗SO2的物质的量和生成SO3的物质的量相同时,反应达到平衡状态 | |
| C. | 充入SO3气体,体系压强增大,平衡向右移动 | |
| D. | 升高温度,平衡向左移动 |
14.下列各种溶液中,能大量共存的无色透明的离子组( )
| A. | 使PH=0的溶液:Fe2+、NO3-、SO42-、I- | |
| B. | C(H+)=10-14mol•L-1的溶液中:Na+、AlO2-、S2-、SO32- | |
| C. | 酸性环境下:Na+、Cu2+、NO3-、SO42- | |
| D. | 使紫色石蕊试液变红的溶液中:K+、Na+、Ca2+、HCO3- |
18.对于溶液中某些离子的检验及结论一定正确的是( )
| A. | 加入足量稀盐酸无沉淀,再加入氯化钡溶液后有白色沉淀产生,一定有SO42- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 某溶液中加入硝酸银溶液生成白色沉淀,说明溶液中有Cl- | |
| D. | 无色溶液中加入稀盐酸产生无色气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |