题目内容
下列化学方程式中有一个与其他三个在分类上不同,这个反应是( )
A、3Fe+2O2
| ||||
B、C+CO2
| ||||
C、NH4HCO3
| ||||
| D、Na2CO3+CO2+H2O═2NaHCO3 |
考点:化学基本反应类型
专题:物质的性质和变化专题
分析:A、化合反应、氧化还原反应;
B、化合反应、氧化还原反应;
C、分解反应、非氧化还原反应;
D、化合反应、非氧化还原反应.
B、化合反应、氧化还原反应;
C、分解反应、非氧化还原反应;
D、化合反应、非氧化还原反应.
解答:
解:A、化合反应、氧化还原反应;
B、化合反应、氧化还原反应;
C、分解反应、非氧化还原反应;
D、化合反应、非氧化还原反应,
ABD属于化合反应,C属于分解反应,
故选C.
B、化合反应、氧化还原反应;
C、分解反应、非氧化还原反应;
D、化合反应、非氧化还原反应,
ABD属于化合反应,C属于分解反应,
故选C.
点评:本体考查了化学基本反应类型,题目难度不大,“一变多'为分解反应,“多变一“为化合反应.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
下列图示与对应的叙述相符的是( )
A、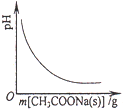 向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 |
B、 向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
C、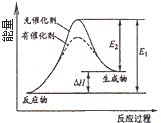 催化剂能改变化学反应的焓变 |
D、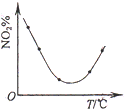 等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 |
某化合物的结构(键线式)及球棍模型如下.该有机分子的核磁共振波谱图如下(单位是ppm):
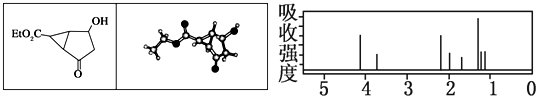
下列关于该有机物的叙述正确的是( )

下列关于该有机物的叙述正确的是( )
| A、右图中最强吸收峰与最弱吸收峰高度比为3:2 |
| B、该有机物分子中含有4个手性碳原子 |
| C、键线式中的Et代表的基团为-CH3 |
| D、该有机物在一定条件下能够发生消去反应和取代反应,但不能发生还原反应 |
将1mol X和1mol Y充入2L密闭容器中发生反应:X(g)+3Y(g)?2Z(s)+a Q(g).2min达到平衡时生成0.4mol Z,测得Q的浓度为0.2mol/L,下列叙述错误的是( )
| A、增大该体系的压强,平衡不移动,化学平衡常数不变 |
| B、反应速率v(Y)=0.15 mol/(L?min) |
| C、Y的平衡转化率为60% |
| D、增加X,平衡向右移动,X的平衡转化率减小 |
下列有机物分子在核磁共振氢谱中只给出一种信号的是( )
| A、HCHO |
| B、CH3OH |
| C、HCOOH |
| D、CH3COOCH3 |
下列关于物质性质与应用的说法正确的是( )
| A、碳具有还原性,高温条件下能将二氧化硅还原为硅 |
| B、二氧化硫有漂白、杀菌性能,可在食品加工中大量使用 |
| C、二氧化硅是半导体材料,可将太阳能直接转化为电能 |
| D、二氧化锰具有较强的氧化性,可作H2O2分解的氧化剂 |
工业制硫酸中的一步重要反应是SO2在400-500℃下的催化氧化,2SO2(g)+O2(g)?2SO3(g),这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是( )
| A、达到平衡时,SO2的浓度与SO3的浓度相等 |
| B、相同状况下,反应2SO3(g)?2SO2(g)+O2(g)是一个吸热反应 |
| C、为了提高SO2转化率,可适当提高O2浓度 |
| D、升高温度,放热反应的速率增大,吸热反应的速率也增大 |
Na2CO3俗名为纯碱,下面对纯碱采用不同分类法进行分类,不正确的是( )
| A、碱 | B、盐 | C、钠盐 | D、碳酸盐 |
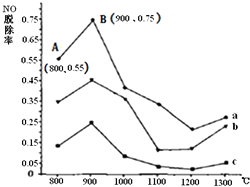 燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.
燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.