题目内容
下列叙述正确的是( )
| A、16 g CH4与18 g NH4+所含质子数相等 |
| B、32S与33S的核外电子数相等,是同一种核素 |
| C、质量相等、体积不等的N2和C2H4的分子数相等 |
| D、同素异形体之间的转化是物理变化 |
考点:核素,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:A.甲烷中含有10个质子,铵离子中含有11个质子;
B.质量数不同,则中子数不同,是不同的核素;
C.根据n=
计算;
D.同素异形体是同种元素的不同单质.
B.质量数不同,则中子数不同,是不同的核素;
C.根据n=
| m |
| M |
D.同素异形体是同种元素的不同单质.
解答:
解:A.16g CH4与18g NH4+的物质的量都是1mol,1mol甲烷中含有10mol质子,1mol铵离子中含有11mol质子,故A错误;
B.32S与33S质量数不同,则中子数不同,是同种元素的不同的核素,故B错误;
C.N2和C2H4的摩尔质量都是28g/mol,质量相同,由n=
可知,物质的量相同,则分子数相同,故C正确;
D.同素异形体是同种元素的不同单质,则同素异形体之间的转化是化学变化,故D错误.
故选C.
B.32S与33S质量数不同,则中子数不同,是同种元素的不同的核素,故B错误;
C.N2和C2H4的摩尔质量都是28g/mol,质量相同,由n=
| m |
| M |
D.同素异形体是同种元素的不同单质,则同素异形体之间的转化是化学变化,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的应用、原子的结构、同素异形体等,侧重于基础知识的考查,本题难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、水玻璃、漂白粉、胆矾均为混合物 |
| B、生成盐和水的反应一定是中和反应 |
| C、NaOH、MgC12、NaC1O、NH4C1均为含共价键的离子化合物 |
| D、煤经过气化或液化两类化学变化过程,可变为清洁能源 |
下列Cl-的物质的量浓度与100mL 0.5mol?L-1 NaCl溶液相同的是( )
| A、100mL 0.5mol?L-1 MgCl2溶液 |
| B、200mL 0.25mol?L-1 AlCl3溶液 |
| C、50mL 1mol?L-1 NaCl溶液 |
| D、25mL 0.5mol?L-1 HCl溶液 |
同体积、同物质的量浓度的几种可溶性盐的溶液中,一定含有相同的( )
| A、溶质的物质的量 |
| B、溶质的质量 |
| C、酸根离子数 |
| D、金属离子数 |
下列物质的名称、俗名与化学式完全对应的是( )
| A、氢氧化钙 熟石灰 CaO |
| B、碳酸钙 生石灰 CaCO3 |
| C、氯化钠 食盐 NaCl |
| D、汞 水银 Ag |
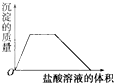
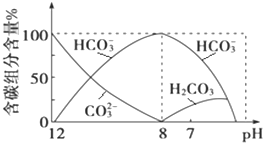 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.