题目内容
下列电离方程式中,书写正确的是( )
| A、KClO3=K++Cl-+3O2- |
| B、NaHCO3=Na++H++CO32ˉ |
| C、NaHSO4=Na++H++SO42ˉ |
| D、FeCl3=Fe3++Clˉ |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式.离子所带电荷数一般可根据它们在化合物中的化合价来判断.所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等.
解答:
解:A、含有原子团的物质电离时,原子团应作为一个整体,不能分开,氯酸根不能分,则电离方程式为KClO3=K++ClO3-,故A错误;
B、碳酸氢根离子不能拆开,该离子方程式为:NaHCO3=Na++HCO3-,故B错误;
C、NaHSO4=Na++H++SO42-,电荷守恒、离子符号正确,所以电离方程式书写正确,故C正确;
D、离子方程式电荷不守恒,该离子方程式为:FeCl3=Fe3++3Cl-,故D错误.
故选C.
B、碳酸氢根离子不能拆开,该离子方程式为:NaHCO3=Na++HCO3-,故B错误;
C、NaHSO4=Na++H++SO42-,电荷守恒、离子符号正确,所以电离方程式书写正确,故C正确;
D、离子方程式电荷不守恒,该离子方程式为:FeCl3=Fe3++3Cl-,故D错误.
故选C.
点评:本题考查了电离方程式的正误判断,解此类题时,首先分析应用的原理是否正确,然后再根据离子方程式的书写规则进行判断.

练习册系列答案
相关题目
下列化学变化生成物总能量比反应物总能量高的是( )
①生石灰与水反应
②铝与盐酸反应
③氯化铵与Ba(OH)2?8H20反应
④石灰石高温分解
⑤氢气与氧气反应生成H20.
①生石灰与水反应
②铝与盐酸反应
③氯化铵与Ba(OH)2?8H20反应
④石灰石高温分解
⑤氢气与氧气反应生成H20.
| A、①③④ | B、②⑨④ |
| C、②③ | D、③④ |
下列叙述正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” | |||
B、对于可逆反应N2(g)+3H2(g)
| |||
| C、硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 | |||
| D、阴极射线和α-粒子散射现象都对原子结构模型的建立做出了贡献 |
在V L Al2(SO4)3溶液中加入过量氨水,过滤得沉淀,然后在高温中灼烧沉淀最后得到白色固体mg,溶液中SO42-的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列化学用语表述正确的是( )
| A、蔗糖的分子式:C6H12O6 |
B、NH3的电子式: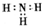 |
C、甲烷的比例模型: |
| D、二氧化碳的结构式:O-C-O |
在18℃时,H2SO3的Kl=1.5×10-2、K2=1.0×10-7,H2S的Kl=9.1×10-8、K2=1.1×10-12,则下列说法中正确的是( )
| A、亚硫酸的酸性弱于氢硫酸 |
| B、亚硫酸溶液的酸性一定强于氢硫酸溶液 |
| C、氢硫酸的酸性弱于亚硫酸 |
| D、多元弱酸的酸性主要由第二步电离决定 |
下列反应中属于氧化还原反应的是( )
| A、CO2+2NaOH═Na2CO3+H2O |
| B、CuO+2HCl═CuCl2+H2O |
| C、CaCO3+2HCl═CaCl2+H2O+CO2↑ |
| D、2Na+2H2O═2NaOH+H2↑ |
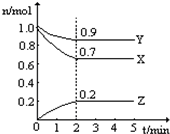 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: