题目内容
13.足量NaHSO3溶液和Na2CO3溶液混合后能产生CO2气体,下列说法中正确的是( )| A. | 反应的离子方程式:2H++CO32-═H2O+CO2↑ | |
| B. | 若向Na2CO3溶液中通入足量的SO2气体,也可得到CO2 | |
| C. | HSO3-的水解程度大于其电离程度 | |
| D. | 各级电离常数:K1(H2SO3)>K1(H2CO3)>K2(H2SO3)>K2(H2CO3) |
分析 NaHSO3溶液和Na2CO3溶液混合加热煮沸,亚硫酸氢钠溶液中亚硫酸氢根离子电离大于水解程度,溶液显酸性,和碳酸钠反应生成二氧化碳生CO2气体,说明亚硫酸氢根的电离程度大于碳酸,由此分析解答;
解答 解:A、亚硫酸氢根是多元弱酸根,所以反应的离子方程式:2HSO3-+CO32-═H2O+CO2↑+2SO32-,故A错误;
B、亚硫酸的酸性强于碳酸,所以向Na2CO3溶液中通入足量的SO2气体,也可得到CO2,故B正确;
C、HSO3-的水解程度水于其电离程度,故C错误;
D、各级电离常数应是:K1(H2SO3)>K2(H2SO3)>K1(H2CO3)>K2(H2CO3),故D错误;
故选B.
点评 本题考查了盐溶液中 离子浓度变化分析,电离和水解的分析判断,应用强制弱是解题关键,题目难度中等.

练习册系列答案
相关题目
3.关于下列氧化还原反应的说法正确的是( )
| A. | 在2Al+2NaOH+2H2O═2NaAlO2+3H2反应中,水和氢氧化钠均作氧化剂 | |
| B. | Al分别于盐酸和氢氧化钠溶液反应,生成等质量的H2,转移的电子数相同 | |
| C. | CO2与Na2O2反应中,每生成1molO2,转移4mol电子 | |
| D. | 在Cu2S+4H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+S↓+SO2↑+4H2O反应中,被氧化的元素只有硫 |
4.进行化学实验时应强化安全意识.下列做法正确的是( )
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 加热碳酸氢钠固体时使试管竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 实验室制取少量的氯气,在通风橱内进行 |
1.为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是( )
| 选项 | 物质 | 试剂 | 分离方法 |
| A | Cl2(水蒸气) | 生石灰 | 洗气 |
| B | KCl溶液(K2SO4) | 适量Ba(NO3)2溶液 | 过滤 |
| C | NaCl固体(KNO3) | 蒸馏水 | 冷却结晶 |
| D | 花生油(水) | - | 分液 |
| A. | A | B. | B | C. | C | D. | D |
8.将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生0.04mol H2,残留固体1.28g.过滤,滤液中无Cu2+,测得滤液中n(H+)为0.08mol.则原混合物中单质铁的质量是( )
| A. | 2.24g | B. | 3.36g | C. | 5.60g | D. | 10.08g |
18.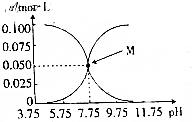 常温下,有c(HCN)+c(CN-)=0.1mol•L-1的氢氰酸、氰化钠的混合溶液,溶液中c(HCN)、c(CN-)与pH的关系如图所示,下列叙述错误的是( )
常温下,有c(HCN)+c(CN-)=0.1mol•L-1的氢氰酸、氰化钠的混合溶液,溶液中c(HCN)、c(CN-)与pH的关系如图所示,下列叙述错误的是( )
 常温下,有c(HCN)+c(CN-)=0.1mol•L-1的氢氰酸、氰化钠的混合溶液,溶液中c(HCN)、c(CN-)与pH的关系如图所示,下列叙述错误的是( )
常温下,有c(HCN)+c(CN-)=0.1mol•L-1的氢氰酸、氰化钠的混合溶液,溶液中c(HCN)、c(CN-)与pH的关系如图所示,下列叙述错误的是( )| A. | 在pH=8.75的该溶液中:c(CN-)>c(HCN)>c(OH-)>c(H+) | |
| B. | 在M点所表示的溶液中:c(Na+)+c(H+)=c(HCN)+c(OH-) | |
| C. | 该溶液呈酸性、碱性或中性时,始终有:c(Na+)+c(H+)+c(OH-)-c(HCN)=0.1mol•L-1 | |
| D. | 该溶液中当c(HCN)=c(CN-)时,盐的水解程度大于酸的电离程度 |
5.短周期元素W、X、Y、Z的原子序数依次增大,W的原子半径最小,X的最外层电子数是次外层的3倍,其中W与Y、X与Z分别同主族,任意3种元素组成的物质中不能破坏水的电离平衡的有( )
| A. | 1种 | B. | 3种 | C. | 4种 | D. | 5种 |
9.一化学研究性学习小组对某Na2CO3和NaHC:O3的混合溶液(以下简称“样品溶液”)的组成进行探究.取20.0mL样品溶液不断滴入1.0mol•L-1的稀盐酸,加入盐酸的体积和产生的现象见表.
回答下列有关问题:
(1)配制1.0mol•L-1的稀盐酸250mL,需要36.5%的浓盐酸20.8mL(36.5%的浓盐酸的密度约为1.2g•cm-3);实验配制过程中所用的玻璃仪器除烧杯、玻璃棒和量筒外,还有250mL容量瓶、胶头滴管.
(2)第Ⅱ阶段溶液中反应的离子方程式为:HCO3-+H+=H2O+CO2↑.样品溶液中c(CO32-)=0.500mol•L-1mol•L-1.
| 反应阶段 | I | II | III |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 产生气体 | 无气体 |
| 解释 | CO32-+H+=HCO3- |
(1)配制1.0mol•L-1的稀盐酸250mL,需要36.5%的浓盐酸20.8mL(36.5%的浓盐酸的密度约为1.2g•cm-3);实验配制过程中所用的玻璃仪器除烧杯、玻璃棒和量筒外,还有250mL容量瓶、胶头滴管.
(2)第Ⅱ阶段溶液中反应的离子方程式为:HCO3-+H+=H2O+CO2↑.样品溶液中c(CO32-)=0.500mol•L-1mol•L-1.
10.下列物质不能通过化合反应得到的是( )
| A. | Fe(OH)3 | B. | FeCl3 | C. | Al(OH)3 | D. | NaHCO3 |