题目内容
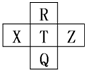 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A、非金属性:T<X<R |
| B、气态氢化物稳定性:R<T<Q |
| C、R与Q的电子数相差16 |
| D、X与Q最高价氧化物的水化物的质子数相差18 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:R单质在暗处与H2剧烈化合并发生爆炸,则R为F元素,由元素R、X、T、Z、Q在元素周期表中的相对位置,可知T为Cl、Q为Br、X为S、Z为Ar,结合元素周期律解答.
解答:
解:R单质在暗处与H2剧烈化合并发生爆炸,则R为F元素,由元素R、X、T、Z、Q在元素周期表中的相对位置,可知T为Cl、Q为Br、X为S、Z为Ar,
A.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性:S<Cl<F,故A错误;
B.同主族自上而下非金属性减弱,氢化物稳定性减弱,即氢化物稳定性:HF>HCl>HBr,故B错误;
C.R为F、Q为Br,二者原子核外电子数相差8+18=26,故C错误;
D.X与Q最高价氧化物的水化物分别为H2SO4、HBrO4,质子数相差为(1+35)-(2+16)=18,故D正确,
故选D.
A.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性:S<Cl<F,故A错误;
B.同主族自上而下非金属性减弱,氢化物稳定性减弱,即氢化物稳定性:HF>HCl>HBr,故B错误;
C.R为F、Q为Br,二者原子核外电子数相差8+18=26,故C错误;
D.X与Q最高价氧化物的水化物分别为H2SO4、HBrO4,质子数相差为(1+35)-(2+16)=18,故D正确,
故选D.
点评:本题考查元素周期表与元素周期律应用,难度不大,注意对元素周期律的理解掌握,理解同主族原子序数关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列分子中,所有原子都在同一条直线上的是( )
| A、C2H2 |
| B、C2H4 |
| C、C2H6 |
| D、CO2 |
将SO2气体通入BaCl2溶液至饱和,无沉淀生成,再通入另一种气体仍没有沉淀生成,则第二次通入的气体可能是下列气体中的( )
①NO2 ②CO2③Cl2 ④HCl ⑤NH3 ⑥H2S.
①NO2 ②CO2③Cl2 ④HCl ⑤NH3 ⑥H2S.
| A、②④⑥ | B、①⑤⑥ |
| C、②④ | D、②③⑤ |
下列各组离子在指定条件下,一定能大量共存的是( )
| A、能使红色石蕊试纸显蓝色的溶液:K+、Na+、SO42-、C2O42- |
| B、能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br- |
| C、水电离出的c(H+)=10-12 mol/L的溶液:Ba2+、Na+、SO3-、S2- |
| D、加入铝条有氢气放出的溶液:Na+、NH4+、Cl-、NO3- |
下列有关化学用语表示正确的是( )
A、N2的电子式: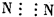 | ||
B、S2-的结构示意图: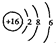 | ||
C、NH4Br的电子式: | ||
D、原子核内有l8个中子的氯原子:
|
下列说法正确的是( )
| A、淀粉和蛋白质它们水解的最终产物都是葡萄糖 |
| B、为防止轮船的船体在海水中被腐蚀,一般在船身连接锌块 |
| C、万一不慎误服重金属盐,应大量吞服鸡蛋清 |
| D、麦芽糖能水解,且最终水解产物有两种 |
下列各物质的名称正确的是( )
| A、1,2-二甲基丁烷 |
| B、2,3,3-三甲基-2-丁烯 |
| C、3,4,4-三甲基-1-戊炔 |
| D、2,3-二甲基苯 |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:1 |
| B、分子个数之比为11:12 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
下列说法正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| B、活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C、氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
| D、绿色化学期望利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放 |