题目内容
1.随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.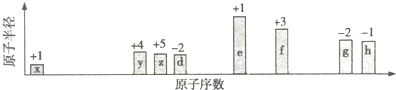
根据判断出的元素回答问题:
(1)八种短周期元素中最高价氧化物对应的水化物碱性最强的元素名称是:钠
(2)比较d、e、f常见离子的半径的从大到小的顺序为(用化学式表示,下同)O2->Na+>Al3+;比较g、h的最高价氧化物对应的水化物的酸性强弱是:HClO4>H2SO4.y、z、d气态氢化物的热稳定性从强到弱的顺序为:H2O>NH3>CH4
(3)f的最高价氧化物对应的水化物分别与e、f最高价氧化物对应的水化物反应的离子方程式为:Al(OH)3+OH-=[Al(OH)4]-、Al(OH)3+3H+═Al3++3H2O;图中元素z的氢化物和它最高价氧化物对应水化物之间发生反应的离子方程式为:NH3+H+═NH4+
(4)下列叙述中一定能说明h元素比g元素非金属性强的是BC
A.h氢化物的水溶液是强酸,而g氢化物水溶液是弱酸
B.h的单质与Fe反应生成物中铁是+3价的;而g单质和Fe反应生成物中铁是+2价
C.h的单质比g的单质更容易和H2化合,而且h生成的氢化物比g稳定性
D.常温时,g的单质熔点比h单质的熔点高.
E.h原子的半径g原子的半径小.
分析 从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素.
(1)元素金属性越强,最高价氧化物对应的水化物碱性越强;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,电子层越多离子半径越大;元素非金属性越强,最高价氧化物对应的水化物的酸性越强;元素非金属性越强,对应氢化物越稳定;
(3)f的最高价氧化物对应的水化物为Al(OH)3,分别与e、f最高价氧化物对应的水化物(强氧化钠、盐酸)反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-,Al(OH)3+3H+═Al3++3H2O;z的氢化物和它最高价氧化物对应水化物之间发生反应的离子方程式为NH3+H+═NH4+;
(4)A.氢化物的水溶液酸性强弱不能比较非金属性;
B.同个还原剂与不同氧化剂反应,根据氧化性强弱判断非金属性强弱;
C.越容易与氢气化合,元素非金属性越强;
D.单质的硬度和熔、沸点属于物理性质,不能比较金属性强弱;
E.半径不能比较非金属性强弱.
解答 解:从图中的化合价、原子半径的大小及原子序数,可知x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素.
(1)元素金属性越强,最高价氧化物对应的水化物碱性越强,根据分析可知钠的金属性最强,
故答案为:钠;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,电子层越多离子半径越大,d是O元素,e是Na元素,f是Al元素,具有相同电子层结构,半径大小顺序为O2->Na+>Al3+;元素非金属性越强,最高价氧化物对应的水化物的酸性越强,非金属性Cl>S,故酸性HClO4>H2SO4;元素非金属性越强,对应氢化物越稳定,非金属性 O>N>C,故稳定性H2O>NH3>CH4,
故答案为:O2->Na+>Al3+;HClO4;H2SO4;H2O>NH3>CH4;
(3)f的最高价氧化物对应的水化物为Al(OH)3,分别与e、f最高价氧化物对应的水化物(强氧化钠、盐酸)反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-,Al(OH)3+3H+═Al3++3H2O;z的氢化物和它最高价氧化物对应水化物之间发生反应的离子方程式为NH3+H+═NH4+,
故答案为:Al(OH)3+OH-=[Al(OH)4]-;Al(OH)3+3H+═Al3++3H2O;NH3+H+═NH4+;
(4)A.氢化物的水溶液酸性强弱不能比较非金属性,故A错误;
B.同个还原剂与不同氧化剂反应,氯气的单质与Fe反应生成物中铁是+3价的;而S单质和Fe反应生成物中铁是+2价,说明氯气氧化性比S强,故氯元素非金属性强于硫,故B正确;
C.越容易与氢气化合,元素非金属性越强,故C正确;
D.单质的硬度和熔、沸点属于物理性质,不能比较金属性强弱,故D错误;
E.半径不能比较非金属性强弱,故D错误.
故答案为:BC.
点评 本题考查结构性质位置关系应用,根据化合价与原子半径推断元素是解题关键,注意对元素周期律的理解掌握.

| A. | 原子最外层电子数≥4的金属元素有6种,元素符号分别是Ge Sn Pb Te Bi Po | |
| B. | 过渡元素全部属于副族元素,全部都是金属元素,它们位于周期表第3纵行至第12纵行 | |
| C. | 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为1或2 | |
| D. | 在元素周期表中位于ⅡB族左右两列元素分别是ⅠB和ⅢB |
| A. | 一定条件下发生分解反应 | B. | 能萃取溴水中的溴 | ||
| C. | 光照条件下与Cl2发生取代反应 | D. | 能使酸性高锰酸钾溶液褪色 |
已知:①NiO2有强氧化性,可与浓盐酸反应;
②NiCl2易溶于水,Fe3+不能氧化Ni2+.
③某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 2.0×10-32 | 4.1 | - |
| Fe(OH)3 | 3.5×10-38 | 2.2 | 3.5 |
| Fe(OH)2 | 1.0×10-15 | 7.5 | 9.5 |
| Ni(OH)2 | 6.5×10-18 | 6.4 | 8.4 |
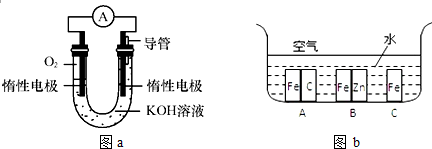
(1)该电池的正极反应式为;NiO2+2H2O+2e-=Ni(OH)2+2OH-;
(2)维持电流强度为1.0A,消耗0.28gFe,理论电池工作965s.(已知F=96500C/mol)
(3)对该电池电极材料进行回收方案设计:
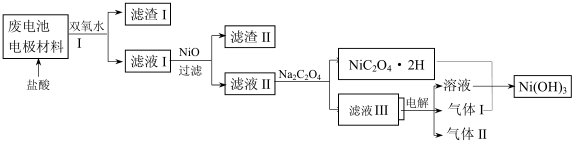
①方案中加入适量双氧水的目的是将溶液中的Fe2+氧化为Fe3+;,;将混合物加入氢氧化钠溶液充分溶解、过滤、洗涤得到滤渣为氢氧化铁,将滤液中通入过量二氧化碳气体过滤洗涤得到沉淀氢氧化铝;在滤液I中慢慢加入NiO固体,则依次析出沉淀Fe(OH)3和沉淀Al(OH)3(填化学式).若两种沉淀都析出,pH应控制在不超过6.4(离子浓度小于1×10-5mol/L为完全沉淀,lg2=0.3、lg3=0.4);设计将析出的沉淀混合物中的两种物质分离开来的实验方案将混合物加入NaOH溶液中充分溶解,过滤、洗涤,滤渣为Fe(OH)3,将滤液通入足量CO2,过滤、洗涤,得沉淀物Al(OH)3.
②滤液III中溶质的主要成分是NaCl(填化学式);气体I为Cl2,判断依据是电解池阳极产生Cl2将NiC2O4氧化为Ni(OH)3.
| A. | 甲烷分子的球棍模型: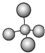 | |
| B. | $\underset{\stackrel{1}{\;}}{1}\underset{\stackrel{\;}{H}}{\;}$、$\underset{\stackrel{2}{\;}}{1}\underset{\stackrel{\;}{H}}{\;}$为同素异形体 | |
| C. | 离子结构示意图 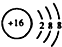 可以表示32S2-,又可以表示34S2- 可以表示32S2-,又可以表示34S2- | |
| D. | 中子数为146、质子数为92的铀(U)原子 14692U |
| A. | 生成乙烯的是氢氧化钾的水溶液 | B. | 生成乙醇的是氢氧化钾的水溶液? | ||
| C. | 生成乙烯的是在170℃下进行的 | D. | 生成乙醇的是氢氧化钾的醇溶液? |
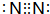 .
.