题目内容
 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.(1)已知NCl3+3H2O═NH3+3HClO,该反应无化合价变化,则电负性N
(2)NH3能与众多过渡元素离子形成配合物,例如往CoCl3溶液中加入氨气,可以得到六配位的配合物CoCl3?x NH3,已知1mol的该配合物与足量AgNO3反应,得到2mol AgCl沉淀,则配合物的化学式为
(3)NF3的结构与NH3类似,但是NF3难以与过渡金属形成配位键,其原因在于
(4)N2H4分子可视为NH3分子中的一个氢原子被-NH2取代形成的另一种氮的氢化物.N2H4分子中氮原子轨道的杂化类型是
(5)N3-为叠氮根,与CO2为等电子体,1mol N3-中含有
考点:元素电离能、电负性的含义及应用,配合物的成键情况,晶胞的计算
专题:
分析:(1)已知NCl3+3H2O═NH3+3HClO,该反应无化合价变化,所以NCl3中氮为-3价,氯为+1价;
(2)1mol的该配合物与足量AgNO3反应,得到2mol AgCl沉淀,说明1mol的氯离子作为配体,而可以得到六配位的配合物,所有5mol的氨气作配体;
(3)从F原子的电负性的角度分析;
(4)根据价层电子对互斥理论确定分子空间构型和原子的杂化方式;
(5)与CO2为等电子体,结构相似,而1molCO2中2molr的π键,先手判断X为Sc元素,利用均摊法计算.
(2)1mol的该配合物与足量AgNO3反应,得到2mol AgCl沉淀,说明1mol的氯离子作为配体,而可以得到六配位的配合物,所有5mol的氨气作配体;
(3)从F原子的电负性的角度分析;
(4)根据价层电子对互斥理论确定分子空间构型和原子的杂化方式;
(5)与CO2为等电子体,结构相似,而1molCO2中2molr的π键,先手判断X为Sc元素,利用均摊法计算.
解答:
解:(1)已知NCl3+3H2O═NH3+3HClO,该反应无化合价变化,所以NCl3中氮为-3价,氯为+1价,所以氮的电负性强于氯,故答案为:>;
(2)1mol的该配合物与足量AgNO3反应,得到2mol AgCl沉淀,说明1mol的氯离子作为配体,而可以得到六配位的配合物,所有5mol的氨气作配体,故答案为:[Co(NH3)5Cl]Cl2;
(3)F原子的电负性较强,氮原子上的孤对电子偏向F原子,而难以形成配位键,故答案为:F原子电负性强,吸引N原子的电子,使其难以给出电子对形成配位键;
(4)NH3分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型;N2H4分子中氮原子的加成电子对=3+1=4,含有一个孤电子对,N原子轨道的杂化类型是sp3,故答案为:sp3;
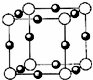
(5)与CO2为等电子体,结构相似,而1molCO2中2molr的π键,X3+所含电子=3+18=21,所以X为21号Sc元素,从图上看○少●多,结合X3N知,○为N3-,以顶角上的○为中心,距离最近的X+有3个.构成一个完整的三维空间需8个这样的立方体,则每个N3-周围有X+:8×3×
=6个(棱上原子为4个晶胞所共用,所以每个原子在此晶胞中为
份),故答案为:2NA,Sc(N3)3,6个.
(2)1mol的该配合物与足量AgNO3反应,得到2mol AgCl沉淀,说明1mol的氯离子作为配体,而可以得到六配位的配合物,所有5mol的氨气作配体,故答案为:[Co(NH3)5Cl]Cl2;
(3)F原子的电负性较强,氮原子上的孤对电子偏向F原子,而难以形成配位键,故答案为:F原子电负性强,吸引N原子的电子,使其难以给出电子对形成配位键;
(4)NH3分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型;N2H4分子中氮原子的加成电子对=3+1=4,含有一个孤电子对,N原子轨道的杂化类型是sp3,故答案为:sp3;
(5)与CO2为等电子体,结构相似,而1molCO2中2molr的π键,X3+所含电子=3+18=21,所以X为21号Sc元素,从图上看○少●多,结合X3N知,○为N3-,以顶角上的○为中心,距离最近的X+有3个.构成一个完整的三维空间需8个这样的立方体,则每个N3-周围有X+:8×3×
| 1 |
| 4 |
| 1 |
| 4 |
点评:本题考查较为综合,涉及分子空间构型以及杂化类型的判断等知识,题目难度较大,注意相关基础的把握和方法的积累.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
除去混在Na2CO3粉末中的少量NaHCO3最合理的方法是( )
| A、加热 |
| B、加NaOH溶液 |
| C、加盐酸 |
| D、加CaCl2溶液 |
下列说法正确的是( )
①通过丁达尔效应可以鉴别稀豆浆和Fe(OH)3胶体
②常温时,FeCl3溶液中Fe3+与Cl-的个数之比等于1:3
③化学方程式Br2+2KI=2KBr+I2说明Br的非金属性强于I
④常温时,0.1mol?L-1盐酸中由水电离出的c(H+)<10-7mol?L-1.
①通过丁达尔效应可以鉴别稀豆浆和Fe(OH)3胶体
②常温时,FeCl3溶液中Fe3+与Cl-的个数之比等于1:3
③化学方程式Br2+2KI=2KBr+I2说明Br的非金属性强于I
④常温时,0.1mol?L-1盐酸中由水电离出的c(H+)<10-7mol?L-1.
| A、①② | B、③④ | C、①③ | D、②④ |
下列各组物质不用任何外加试剂,只用胶头滴管和试管就能鉴别的是( )
| A、AgNO3溶液和NaCl溶液 |
| B、BaCl2溶液和KHSO4溶液 |
| C、NaHCO3溶液和盐酸 |
| D、Na2CO3溶液和盐酸 |
下列说法不正确的是( )
A、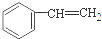 没有顺反异构体 没有顺反异构体 |
| B、1,3-丁二烯可以作为合成高分子化合物的原料 |
| C、用乙醇和浓硫酸制备乙烯时,用水浴加热控制反应温度 |
| D、常温下,将苯酚加入到少量水中有浑浊,滴入适量NaOH溶液后浑浊消失 |
E、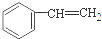 |
下列各化合物的命名正确的是( )
| A、CH2=CH-CH=CH2 1,3-二丁烯 |
B、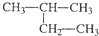 2-甲基丁烷 2-甲基丁烷 |
C、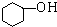 苯酚 苯酚 |
D、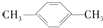 间二甲苯 间二甲苯 |
下列有关阿伏加德罗常数(NA)的说法正确的是( )
| A、32 g O2所含的原子数目为NA |
| B、1 mol氢约含有6.02×1023个微粒 |
| C、标准状况下,2NA 个H2O的体积约为44.8 L |
| D、标准状况下,22.4 L CH4和H2的混合气体中含有NA个分子 |