题目内容
下列叙述正确的是( )
| A、甲醛分子空间构型为平面三角形,而CO2为直线形,CH4为正四面体形 |
| B、甲醛和CO2分子中的中心原子均采取sp2杂化,而NH3分子中采取sp3杂化 |
| C、苯是非极性分子,且分子中σ键和π键的个数比为3:1 |
| D、CO2晶体的熔点、沸点都比二氧化硅晶体的低 |
考点:判断简单分子或离子的构型,共价键的形成及共价键的主要类型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:根据价层电子对互斥理论确定分子空间构型及中心原子杂化方式,价层电子对个数=配原子个数+孤电子对个数.
解答:
解:A、甲醛中心原子C上无孤电子对,价层电子对数为3,空间构型为平面三角形,CO2中心原子C上无孤电子对,价层电子对数为2,空间构型为直线形,CH4中心原子C上无孤电子对,价层电子对数为4,空间构型为正四面体形,故A正确;
B、甲醛中心原子C的价层电子对数为3,采取sp2杂化,CO2中心原子C上无孤电子对,价层电子对数为2,采取sp2杂化,NH3分子中N上含有1个孤电子对,价层电子对数为4,采取sp3杂化,故B错误;
C、苯是非极性分子,分子中含有6个C-H σ键 6个C-C σ键,含有一个大π键,所以σ键和大π键的个数比为12:1,故C错误;
D、二氧化碳晶体为分子晶体,二氧化硅为原子晶体,原子晶体熔沸点高于分子晶体,故D正确;
故选AD.
B、甲醛中心原子C的价层电子对数为3,采取sp2杂化,CO2中心原子C上无孤电子对,价层电子对数为2,采取sp2杂化,NH3分子中N上含有1个孤电子对,价层电子对数为4,采取sp3杂化,故B错误;
C、苯是非极性分子,分子中含有6个C-H σ键 6个C-C σ键,含有一个大π键,所以σ键和大π键的个数比为12:1,故C错误;
D、二氧化碳晶体为分子晶体,二氧化硅为原子晶体,原子晶体熔沸点高于分子晶体,故D正确;
故选AD.
点评:本题考查了微粒空间构型及原子杂化方式,根据价层电子对互斥理论来分析解答即可,难点的孤电子对个数的计算方法,为常考查点,要熟练掌握.

练习册系列答案
相关题目
绿色化学的核心理念是:从源头上减少和消除工业生产对环境的污染,使反应物的原子尽可能全部转化为期望的最终产物.下列做法不符合绿色化学理念的是( )
| A、用水溶剂涂料替代有机溶剂涂料 | ||||
| B、用可降解塑料生产快餐盒 | ||||
C、用Cu+2H2SO4(浓)
| ||||
D、用  制备环氧乙烷 制备环氧乙烷 |
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中.然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.由此可见( )
| A、NH4HCO3和盐酸的反应是放热反应 |
| B、该反应中,热能转化为产物内部的能量 |
| C、反应物的总能量高于生成物的总能量 |
| D、反应的热化学方程式为NH4HCO3+HCl-→NH4Cl+CO2↑+H2O△H=+Q kJ?mol-1 |
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、在常温常压下,11.2 L N2含有的分子数为0.5 NA |
| B、在常温常压下,1 mol Ne含有的原子数为NA |
| C、1 L 1 mol/L醋酸溶液中离子总数为2NA |
| D、18 g水中所含的电子数为8NA |
酸雨是指pH<5.6的雨水.你认为减少酸雨产生的途径可采取的措施是:( )
①用煤作燃料,②把工厂烟囱造高,③燃料脱硫处理,④开发新能源,⑤在已酸化的土壤中加石灰.
①用煤作燃料,②把工厂烟囱造高,③燃料脱硫处理,④开发新能源,⑤在已酸化的土壤中加石灰.
| A、①②③ | B、②③④⑤ |
| C、③④ | D、③④⑤ |
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示.下列判断中,不正确的是( )
| 甲 | 乙 | 丙 | 丁 | ||
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | α3 | |
| A、乙中反应的平衡常数与丁中反应的平衡常数相等 |
| B、该温度下,甲中反应的平衡常数K为200 |
| C、SO2的平衡转化率:α2>α1 |
| D、容器中SO3的物质的量浓度:丙=丁 |
取0.2mol/L HX溶液与0.2mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8(25°C),则混合溶液中下列说法(或关系式)不正确的是( )
| A、由水电离出的c(OH-)=1×10-6 mol/L |
| B、c(Na+)=c(X-)+c(HX) |
| C、c(Na+)-c(OH-)=c(X-)-c(H+) |
| D、c(X-)=c(Na+)>c(OH-)=c(H+) |
下列有关物质结构的表述正确的是( )
A、次氯酸的电子式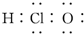 ? ? |
| B、二氧化硅的分子式SiO2 |
C、硫原子结构示意图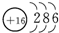 |
D、钠离子的结构示意图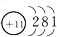 |