题目内容
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入的铁粉质量相等,则原溶液中H+和Cl-的物质的量之比为( )
| A、1:4 | B、1:7 |
| C、1:8 | D、2:5 |
考点:化学方程式的有关计算
专题:计算题
分析:在盐酸和氯化铜的混合溶液中加入足量的铁粉,分别发生:2H++Fe=Fe2++H2↑,Fe+Cu2+=Fe2++Cu,其充分反应,所得滤渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,令Cu的质量为64g,其物质的量为1mol,根据方程式计算溶液中n(H+)、n(Cu2+),再根据电荷守恒可得n(Cl-)=n(H+)+2n(Cu2+),离子浓度之比等于其物质的量之比.
解答:
解:在盐酸和氯化铜的混合溶液中加入足量的铁粉,分别发生:2H++Fe=Fe2++H2↑,Fe+Cu2+=Fe2++Cu,其充分反应,所得滤渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,令Cu的质量为64g,其物质的量为1mol,
Fe+Cu2+=Fe2++Cu
56g 1mol 64g 故溶液中n(Cu2+)=1mol
故与酸反应的Fe的质量为64g-56g=8g,其物质的量为
=
mol,由2H++Fe=Fe2++H2↑,可知n(H+)=
mol,
根据电荷守恒可得n(Cl-)=n(H+)+2n(Cu2+)=
mol+2mol=
mol,
故原混合溶液中c(H+):c(Cl-)=
mol:
mol=1:8,
故选C.
Fe+Cu2+=Fe2++Cu
56g 1mol 64g 故溶液中n(Cu2+)=1mol
故与酸反应的Fe的质量为64g-56g=8g,其物质的量为
| 8g |
| 56g/mol |
| 1 |
| 7 |
| 2 |
| 7 |
根据电荷守恒可得n(Cl-)=n(H+)+2n(Cu2+)=
| 2 |
| 7 |
| 16 |
| 7 |
故原混合溶液中c(H+):c(Cl-)=
| 2 |
| 7 |
| 16 |
| 7 |
故选C.
点评:本题考查化学方程式计算、混合物有关计算,属于无数据型计算,注意利用赋值法进行解答,明确发生的反应是根据,难度中等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
我国高速铁路技术世界领先.高速铁路的无缝钢轨是将钢轨间的接头用铝与四氧化三铁发生铝热反应进行焊接而成的.下列有关该反应的说法中正确的是( )
| A、每生成1mol铁,转移电子3mol |
| B、Al被还原 |
| C、Fe3O4发生氧化反应 |
| D、Al是还原剂 |
用铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率加快的是( )
| A、滴加少量硫酸铜溶液 |
| B、增多铁片的用量 |
| C、改用98%的浓硫酸 |
| D、加入少量的CH3COONa固体 |
下列离子方程式书写正确的是( )
| A、将少量SO2气体通入NaClO溶液中 SO2+2ClO-+H2O=SO32-+2HClO |
| B、向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7 Ba2++OH-+H++SO42-=BaSO4↓+2H2O |
| C、向Ca(H2PO4)2溶液中滴入过量的NaOH溶液 3Ca2++6H2PO4-+12OH-=Ca3(PO4)2↓+4PO43-+12H2O |
| D、112mL(标况)Cl2通入10mL1mol/L的FeBr2溶液中 2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
下列实验装置图正确的是( )
A、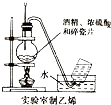 |
B、 |
C、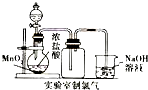 |
D、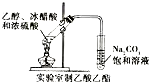 |
在甲、乙两个体积不同的密闭容器中,分别充入质量相同的CO、CO2气体时,两容器的温度和压强均相同,则下列说法正确的是( )
| A、充入的CO分子数比CO2分子数少 |
| B、甲容器的体积比乙容器的体积小 |
| C、CO的摩尔体积比CO2的摩尔体积小 |
| D、甲中CO的密度比乙中CO2的密度小 |
