题目内容
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液,选择甲基橙作指示剂.请填写下列空白:(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.振荡锥形瓶时部分液体溅出
D.读取盐酸体积时,开始俯视读数,滴定结束时仰视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示所用盐酸溶液的体积为
考点:中和滴定
专题:实验题
分析:(1)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化;
(2)根据c(待测)=
分析误差;
(3)根据滴定管的结构和精确度以及测量的原理;
(2)根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
(3)根据滴定管的结构和精确度以及测量的原理;
解答:
解:(1)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化;
故答案为:锥形瓶中溶液颜色变化;
(2)A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,标准液浓度偏小,会导致测定标准液体积偏高,测定值偏高,故A错误;
B.锥形瓶水洗后未干燥,待测液的物质的量不变,标准液体积不变,测定值不变,故B错误;
C.振荡锥形瓶时部分液体溅出,会导致测定标准液体积偏小,测定值偏低,故C正确;
D.读取盐酸体积时,开始俯视读数,滴定结束时仰视读数,会导致测定标准液体积偏大,测定值偏高,故D错误;
故选C.
(3)起始读数为0.00mL,终点读数为25.90mL,盐酸溶液的体积为25.90mL;
故答案为:25.90;
故答案为:锥形瓶中溶液颜色变化;
(2)A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,标准液浓度偏小,会导致测定标准液体积偏高,测定值偏高,故A错误;
B.锥形瓶水洗后未干燥,待测液的物质的量不变,标准液体积不变,测定值不变,故B错误;
C.振荡锥形瓶时部分液体溅出,会导致测定标准液体积偏小,测定值偏低,故C正确;
D.读取盐酸体积时,开始俯视读数,滴定结束时仰视读数,会导致测定标准液体积偏大,测定值偏高,故D错误;
故选C.
(3)起始读数为0.00mL,终点读数为25.90mL,盐酸溶液的体积为25.90mL;
故答案为:25.90;
点评:本题主要考查了中和滴定操作、仪器的使用、误差分析以及计算,难度不大,根据课本知识即可完成.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
如果ag某气体中含有的分子数为b,则cg该气体的物质的量为(设阿伏加德罗常数为NA)( )
A、
| ||
B、
| ||
C、
| ||
D、
|
汽车尾气净化中的一个反应如下:NO(g)+CO(g)?
N2(g)+CO2(g)△H=-373.4kJ?mol-1在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是( )
| 1 |
| 2 |
A、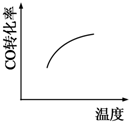 |
B、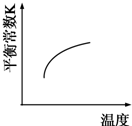 |
C、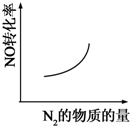 |
D、 |
下列溶液中,微粒的物质的量浓度正确的是( )
| A、在Na2CO3溶液中:c(OH-)+2c(CO32-)+c(HCO3-)=c(H+)+c(Na+) |
| B、常温时,将pH=1的醋酸和pH=13的NaOH溶液等体积混合后的溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、NaHCO3溶液中:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、0.1mol?L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3?H2O)=0.2mol |
室温下,下列各组粒子在指定溶液中能大量共存的是( )
| A、Ba(NO3)2 溶液中:SO2、Na+、NH4+、CH3COO- |
| B、Kw/c(H+)=0.1mol/L-1的溶液中:K+、Ba2+、C1-、HCO3- |
| C、FeCl2溶液中:H2O2、Mg2+、H+、Cl- |
| D、含苯酚的水溶液中用::Al3+、NH4+、Br-、SO42- |
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
| R | ||
| X | Y | Z |
| A、R的气态氢化物比Y的气态氢化物稳定 |
| B、原子半径大小顺序是Z>Y>X |
| C、Y、R形成的化合物YR2能使KMnO4溶液褪色 |
| D、X、Y、Z中X的最高价氧化物对应的水化物的酸性最强 |
下列装置所示的实验中,能达到实验目的是( )
A、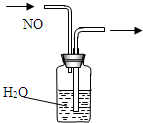 排水集气法收集NO |
B、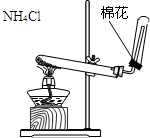 实验室制取氨气 |
C、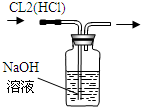 除去氯气中的氯化氢 |
D、 分离碘酒中的碘和酒精 |

 ”的反应中属于取代反应的是
”的反应中属于取代反应的是 中的所有原子是否在同一平面上
中的所有原子是否在同一平面上