题目内容
下列实验操作会引起测定结果偏高的是( )
| A、用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,读取滴定管末读数时,仰视刻度线 |
| B、测定硫酸铜晶体中结晶水含量的实验时,加热时间过短未完全变白 |
| C、中和滴定时,加待测液前锥形瓶内有少量水 |
| D、测定1mol氢气体积的操作中,反应结束后未抽气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.仰视读数导致HCl体积偏大;
B.加热时间过短而使硫酸铜晶体未完全变白,导致结晶水未完全失去;
C.中和测定时,锥形瓶内有少量水不影响待测液溶质的物质的量;
D.测定1mol氢气体积的操作中,反应结束后未抽气,忽略此步骤会导致测量结果偏小.
B.加热时间过短而使硫酸铜晶体未完全变白,导致结晶水未完全失去;
C.中和测定时,锥形瓶内有少量水不影响待测液溶质的物质的量;
D.测定1mol氢气体积的操作中,反应结束后未抽气,忽略此步骤会导致测量结果偏小.
解答:
解:A.滴定管的小刻度在下、大刻度在上,所以仰视读数导致HCl体积偏大,导致最终实验结果偏高,故A正确;
加热时间过短而使硫酸铜晶体未完全变白,导致结晶水未完全失去,水的量偏小,则测定结果偏低,故B错误;
C.中和测定时,锥形瓶内有少量水不影响待测液溶质的物质的量,所以不影响测量结果,故C错误;
D.测定1mol氢气体积的操作中,反应结束后未抽气,忽略此步骤时,导致导气管中部分溶液未被排出,所以会导致测量结果偏低,故D错误;
故选A.
加热时间过短而使硫酸铜晶体未完全变白,导致结晶水未完全失去,水的量偏小,则测定结果偏低,故B错误;
C.中和测定时,锥形瓶内有少量水不影响待测液溶质的物质的量,所以不影响测量结果,故C错误;
D.测定1mol氢气体积的操作中,反应结束后未抽气,忽略此步骤时,导致导气管中部分溶液未被排出,所以会导致测量结果偏低,故D错误;
故选A.
点评:本题考查了化学实验方案评价,涉及实验误差分析,注意:A中滴定管和量筒数值的区别、C中锥形瓶是否需要润洗,这些都是易错点.

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| B、水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C、pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| D、c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
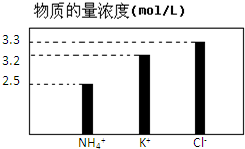 在无土栽培中,需配置20L含NH4Cl、KCl和K2CO3的营养液.营养液中部分离子的物质的量浓度如图所示.若用KCl、NH4Cl和(NH4)2CO3三种固体为原料来配制上述营养液,则需KCl、NH4Cl和(NH4)2CO3三种固体得物质的量依次为(单位为mol)( )
在无土栽培中,需配置20L含NH4Cl、KCl和K2CO3的营养液.营养液中部分离子的物质的量浓度如图所示.若用KCl、NH4Cl和(NH4)2CO3三种固体为原料来配制上述营养液,则需KCl、NH4Cl和(NH4)2CO3三种固体得物质的量依次为(单位为mol)( )| A、2、64、24 |
| B、16、50、24 |
| C、32、50、12 |
| D、64、2、24 |
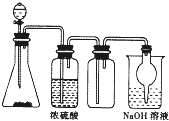 如图是一套实验室制取气体装置,用于发生、干燥、收集和吸收有毒气体,下列各实验能利用这套装置进行的是( )
如图是一套实验室制取气体装置,用于发生、干燥、收集和吸收有毒气体,下列各实验能利用这套装置进行的是( )| A、MnO2和浓盐酸制氯气 |
| B、锌粒和稀硫酸制氢气 |
| C、铜片和浓硝酸制二氧化氮 |
| D、浓氨水和生石灰制氨气 |
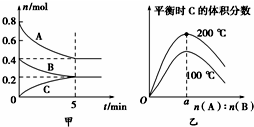 在2L的密闭容器中发生反应xA(g)+yB(g)?zC(g).图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
在2L的密闭容器中发生反应xA(g)+yB(g)?zC(g).图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )| A、200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol?L-1?min-1 |
| B、200℃时,该反应的平衡常数为25 L2/mol2 |
| C、当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大 |
| D、由图乙可知,反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 |
 2013年9月,中国华北华中地区发生了严重的雾霆天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霆形成的原因.
2013年9月,中国华北华中地区发生了严重的雾霆天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霆形成的原因.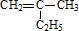 的键线式
的键线式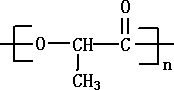 是由一种单体缩聚而成的,该单体的结构简式为
是由一种单体缩聚而成的,该单体的结构简式为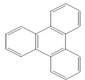 的一氯取代物有
的一氯取代物有