题目内容
10.下列实验方案设计正确的是( )| A. | 分解高锰酸钾制取氧气后,残留在试管内壁上的黑色物质可用浓盐酸洗涤 | |
| B. | 失去标签的AgNO3溶液、稀盐酸、NaOH溶液、AlCl3溶液可选用(NH4)2CO3 溶液作鉴别试剂 | |
| C. | 用铜丝代替铂丝做焰色反应 | |
| D. | 把SO2气体通入酸性KMnO4溶液中,KMnO4溶液的颜色褪去,即可证明SO2具有漂白性 |
分析 A.二氧化锰与浓盐酸反应;
B.AgNO3溶液、稀盐酸、NaOH溶液、AlCl3溶液分别与(NH4)2CO3 溶液反应的现象为:白色沉淀、无色无味气体、刺激性气体、白色沉淀;
C.铜的焰色反应为绿色;
D.SO2气体通入酸性KMnO4溶液中发生氧化还原反应.
解答 解:A.留在试管内壁上的黑色物质为二氧化锰,加热时与浓盐酸反应,可洗涤除去,故A正确;
B.AgNO3溶液、稀盐酸、NaOH溶液、AlCl3溶液分别与(NH4)2CO3 溶液反应的现象为:白色沉淀、无色无味气体、刺激性气体、白色沉淀和气体,能鉴别,故B正确;
C.铜的焰色反应为绿色,则不能用铜丝代替铂丝做焰色反应,故C错误;
D.SO2气体通入酸性KMnO4溶液中发生氧化还原反应,体现二氧化硫的还原性,与漂白性无关,故D错误;
故选AB.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、焰色反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
1.通常所说的三大材料是指金属材料、无机非金属材料和有机高分子材料.下述材料中全部属于金属材料的是( )
| A. | 玻璃、陶瓷、水泥 | B. | 塑料,合成纤维、橡胶 | ||
| C. | 青铜、碳素钢、硬铝 | D. | 玻璃钢、聚乙烯、超导陶瓷 |
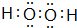 .
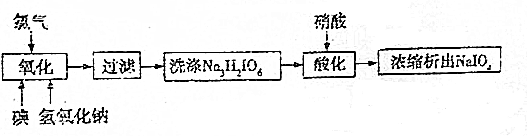
.

 2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )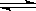 H+(溶液)+In-(溶液,黄色) 而用作酸碱指示剂。往该溶液中加入Na2O2粉末,则溶液颜色为( )
H+(溶液)+In-(溶液,黄色) 而用作酸碱指示剂。往该溶液中加入Na2O2粉末,则溶液颜色为( )