题目内容
3.下列反应无论怎样调整反应物的用量都只能生成一种物质的是( )| A. | 甲烷与氯气混合后光照发生反应 | B. | 乙炔与氯气的加成反应 | ||
| C. | 乙烯与氯化氢的加成反应 | D. | 二氧化碳通入石灰水中 |
分析 A.甲烷光照下的取代反应为连锁式反应;
B.乙炔中含碳碳三键,氯气的量不同,产物不同;
C.乙烯与氯化氢只能以1:1加成;
D.根据石灰水和少量CO2反应的产物是碳酸钙和水,与过量CO2反应的产物是碳酸氢钙.
解答 解:A.甲烷与Cl2在光照条件下发生取代反应可得到各种氯代产物和氯化氢,故A不选;
B.乙炔与Cl2加成反应可以得到CHCl═CHCl或CHCl2CHCl2,故B不选;
C.乙烯与氯化氢以1:1加成,只有一种氯乙烷,故C选;
D.石灰水和少量CO2反应的产物是碳酸钙和水,与过量CO2反应的产物是碳酸氢钙,故D不选.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机反应中官能团变化、结构变化判断反应类型为解答的关键,侧重分析与应用能力及有机反应类型的考查,题目难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
18.将ag Fe2O3、Al2O3样品溶解在过量的200mL 0.05mol/L的硫酸溶液中然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
| A. | 0.1 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.4 mol•L-1 | D. | 0.8 mol•L-1 |
8.常温下,0.1mol•L-1的下列溶液中,有关微粒的物质的量浓度关系正确的是( )
| A. | NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | NaHCO3溶液:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
15.NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.1 mol丙烯酸中含有双键的数目为0.1NA | |
| B. | 常温常压下,Cu、Zn、稀硫酸构成的原电池中,正极产生1.12 L H2时,转移的电子数应为0.1NA | |
| C. | 一定条件下定容容器中充入3molH2(g)和1 mol N2(g)发生反应:H2(g)+N2(g)?2NH3 (g);△H=-QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.75 NA | |
| D. | 在50 g质量分数为46%的乙醇水溶液中,含有的氢原子总数为6NA |
12.下列有关分子晶体熔点高低的叙述中,正确的是( )
| A. | 氯气>碘单质 | B. | 四氯化硅>四氟化硅 | ||
| C. | NH3<PH3 | D. | 异戊烷>正戊烷 |

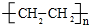 ;
;