题目内容
有一块表面被氧化成氧化钠的金属钠,质量是10.8g,将它投入到100g水中完全反应后,收集到0.2g氢气,得到密度为1.106g/cm3的溶液,试计算:
(1)未被氧化的金属钠的质量是多少克?
(2)反应后所得溶液中溶质的物质的量浓度.(已知氧化钠与水的反应和氧化钙与水的反应类似)
(1)未被氧化的金属钠的质量是多少克?
(2)反应后所得溶液中溶质的物质的量浓度.(已知氧化钠与水的反应和氧化钙与水的反应类似)
考点:有关混合物反应的计算
专题:计算题
分析:(1)根据反应2Na+2H2O=2NaOH+H2↑计算样品中Na的质量;
(2)结合(1)中的金属Na的质量可计算氧化钠的质量,根据氧化钠中Na元素质量分数计算氧化钠中钠元素质量,进而计算Na元素总质量,利用n=
计算其物质的量,再利用钠元素守恒计算生成NaOH的总物质的量,溶液质量=10.8+100g-生成氢气的质量,根据V=
计算溶液体积,再根据c=
计算.
(2)结合(1)中的金属Na的质量可计算氧化钠的质量,根据氧化钠中Na元素质量分数计算氧化钠中钠元素质量,进而计算Na元素总质量,利用n=
| m |
| M |
| m |
| ρ |
| n |
| V |
解答:
解:(1)反应生成氢气的质量为0.2g,则:
2Na+2H2O=2NaOH+H2↑
46 2
m(Na) 0.2g
m(Na)=
=4.6g,
答:未被氧化的金属钠的质量为4.6g.
(2)m(Na2O)=10.8g-4.6g=6.2g,则氧化钠中钠元素的质量=6.2g×
=4.6g,
混合物中n(Na元素)=
=0.4mol,由钠元素守恒,则与水反应生成的总NaOH的物质的量为:n(NaOH)=0.4mol,溶液的质量为:100g+10.8g-0.2g=110.6g,溶液的体积=
=0.1L,故c(NaOH)=
=4mol/L,
答:溶液中溶质NaOH的物质的量浓度为4mol/L.
2Na+2H2O=2NaOH+H2↑
46 2
m(Na) 0.2g
m(Na)=
| 46×0.2g |
| 2 |
答:未被氧化的金属钠的质量为4.6g.
(2)m(Na2O)=10.8g-4.6g=6.2g,则氧化钠中钠元素的质量=6.2g×
| 46 |
| 62 |
混合物中n(Na元素)=
| 4.6g+4.6g |
| 23g/mol |
| 110.6g |
| 1106g/L |
| 0.4mol |
| 0.1L |
答:溶液中溶质NaOH的物质的量浓度为4mol/L.
点评:本题考查混合物计算、化学方程式的相关计算,(2)中关键是计算溶液的体积,难度中等.

练习册系列答案
相关题目
能正确解释下列反应原理的离子方程式是( )
| A、用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+ |
| B、用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O |
| C、用氯化铁溶液腐蚀印刷线路板上的铜:Fe3++Cu=Fe2++Cu2+ |
| D、FeCl3溶液中撒入CaCO3粉末有气泡产生:2Fe3++3CaCO3+3H2O=2Fe(OH)3↓+3Ca2++3CO2↑ |
某同学写出的下列烷烃的名称中,不符合系统命名法的是( )
| A、2,3-二甲基丁烷 |
| B、2,2,3,3-四甲基丁烷 |
| C、2-甲基丙烷 |
| D、2-甲基-2-乙基丁烷 |
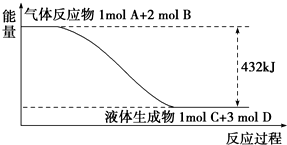 某反应过程中的能量变化如图所示:
某反应过程中的能量变化如图所示: