题目内容
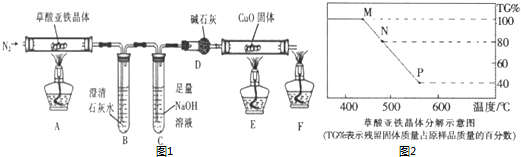
4.常温下,NO、NO2是有毒性气体,既有还原性又有氧化性.NO2的沸点是21℃,-11.2℃时凝固成无色晶体,与NaOH溶液能反应.NO的沸点是-152℃,与NaOH溶液不反应,但与NO2混合时可以与NaOH溶液反应.Ⅰ、某化学实验小组利用如图1装置证明铜和稀硝酸反应产生NO.(加热装置和夹持装置均已略去,气密性已检验,F是用于鼓入空气的打气球).实验操作为:
①将B装置下移,用反应产生的CO2赶走装置中的空气,赶净后,立即将B装置上提.
②将A装置中铜丝放入稀HNO3中,给A装置微微加热.
试回答下列问题:
(1)B仪器的名称是球形干燥管.从装置的设计看,确定E中空气已被赶净的实验现象是装置C中出现白色沉淀.
(2)检验反应产物是NO的实验操作是用F向E中鼓入空气,观察E中气体颜色变化.
(3)D溶液的作用是3H2O2+2NO=2HNO3+2H2O.(用化学方程式表示)
(4)由于E处设计不当,开始收集的气体出现浅的红棕色,你认为该装置如何改正把E中进气管和出气管改为短进长出,保证开始时CO2把空气全部赶出.
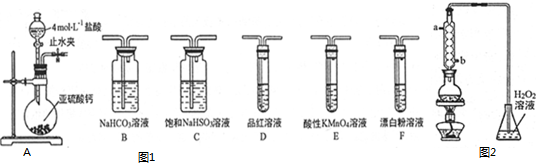
Ⅱ、铜与浓HNO3反应生成NO2,有同学认为可能混有NO,为检验反应产物,该同学利用图2所示的一些装置进行实验.
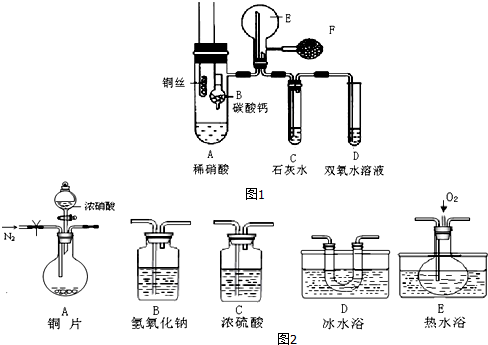
(1)仪器连接顺序为ACDEB.(用字母表示)
(2)证明反应后得到的是NO2和NO混合气体的实验现象是A中产生红棕色气体,气体在D中冷凝为液体,E中无色气体在通入O2后变成红棕色.
(3)已知饱和硝酸铜溶液显蓝色,上述制取NO2得到的溶液却是绿色,有同学分析可能是溶解了NO2,请设计实验验证该结论是否正确取少量饱和硝酸铜溶液于试管中,向该溶液中通入NO2气体,若溶液变绿色,结论正确,反之,不正确.
(或取实验后绿色溶液少量于试管中,加热,若溶液变蓝,则结论正确,反之,不正确).
分析 Ⅰ、图1装置证明铜和稀硝酸反应产生NO.实验时,可先将B装置中CaCO3放入硝酸中,碳酸钙和硝酸反应生成二氧化碳气体,先排出去其中的空气,以便在E烧瓶中收集到NO,以便观察颜色,且在C中可观察到浑浊,有碳酸钙沉淀生成,A中硝酸和铜反应生成NO,易于氧气反应,则将F气球中空气压入E中,有红棕色气体生成,二氧化碳密度比空气重,应用向上排空气法收集,装置D中盛有双氧水,可用与吸收一氧化氮气体,气球F可用于吸收不反应的NO,以防止污染空气,以此解答该题.
(1)根据B装置的特点及其作用分析;从装置的设计看,确定E中空气已被赶尽的实验现象是:装置C中出现白色沉淀;
(2)一氧化氮和氧气反应生成二氧化氮,一氧化氮为无色气体,二氧化氮为红棕色气体,检验反应产物是NO,用F向E中鼓入空气,观察E中气体颜色变化;
(3)过氧化氢具有氧化性,能将+2价的氮氧化成+5价的氮,D溶液的作用是吸收尾气NO;
(4)二氧化碳的密度比空气重,应用向上排空气法收集,把E中进气管和出气管改为短进长出,保证开始时CO2把空气全部赶出.
Ⅱ、铜与浓HNO3反应生成NO2,可能混有NO,检验反应产物.A装置铜和浓硝酸反应,B装置用碱吸收尾气,C装置干燥酸性气体,D装置收集易液化的气体,E通入氧气,可能为NO和氧气反应的装置.
(1)根据实验的目的和各实验装置中盛放的试剂连接装置;
(2)证明反应后得到的是NO2和NO混合气体,需先分离出二氧化氮,然后利用一氧化氮和氧气反应气体的颜色变化检验一氧化氮的存在;
(3)可通过对照实验检验是否溶解了NO2,或将所得溶液进行加热,驱赶溶解的二氧化氮,观察溶液颜色变化进行分析.
解答 解:Ⅰ、(1)B具有球形特征的玻璃仪器为球形干燥管,E中空气已被赶尽时,C中石灰水与二氧化碳反应生成碳酸钙沉淀,可观察到石灰水变浑浊,出现白色沉淀,
故答案为:球形干燥管;装置C中出现白色沉淀;
(2)稀硝酸与铜反应生成硝酸铜和NO,反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,A中硝酸和铜反应生成NO,易与氧气反应,则将F气球中空气压入E中,有红棕色气体生成,如观察到红棕色,则说明生成NO,
故答案为:用F向E中鼓入空气,观察E中气体颜色变化;
(3)NO为有毒气体,D溶液的作用是吸收尾气NO,过氧化氢和一氧化氮发生氧化还原反应:3H2O2+2NO=2HNO3+2H2O,
故答案为:3H2O2+2NO=2HNO3+2H2O;
(4)二氧化碳的密度比空气重,应用向上排空气法收集,故E中应左导管短,右导管长,才有利于排净空气,保证E中全是二氧化碳气体,保证开始时CO2把空气全部赶出,
故答案为:把E中进气管和出气管改为短进长出,保证开始时CO2把空气全部赶出.
Ⅱ、(1)铜与浓HNO3反应生成NO2,可能混有NO,检验反应产物.首先选择A装置:铜与浓HNO3反应,Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,当硝酸浓度变稀,可能发生:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,因产物中有水,会影响后面气体成分的检验,需对气体进行干燥,所以选择C利用浓硫酸对产物气体进行干燥,证明反应后得到的是NO2和NO混合气体,需需先分离出二氧化氮,然后利用一氧化氮和氧气反应气体的颜色变化检验一氧化氮的存在,所以选择装置D,A中产生红棕色气体在D中冷凝为液体,E中无色气体在通入O2后变成红棕色,最后用B吸收尾气,所以连接顺序为:ACDEB,
故答案为:ACDEB;
(2)证明反应后得到的是NO2和NO混合气体,需先分离出二氧化氮,装置D冰水浴,A中产生红棕色气体,气体在D中冷凝为液体,一氧化氮为无色气体,和氧气反应生成红棕色的二氧化氮,所以A中产生红棕色气体,气体在D中冷凝为液体,E中无色气体在通入O2后变成红棕色,可证明反应后得到的是NO2和NO混合气体,
故答案为:A中产生红棕色气体,气体在D中冷凝为液体,E中无色气体在通入O2后变成红棕色;
(3)用对比实验,取少量饱和硝酸铜溶液于试管中,向该溶液中通入NO2气体,若溶液变绿色,结论正确,反之,不正确.或利用气体在温度较高的情况下,溶解度较小的性质,取实验后绿色溶液少量于试管中,加热,若溶液变蓝,则结论正确,反之,不正确,
故答案为:取少量饱和硝酸铜溶液于试管中,向该溶液中通入NO2气体,若溶液变绿色,结论正确,反之,不正确.(或取实验后绿色溶液少量于试管中,加热,若溶液变蓝,则结论正确,反之,不正确).
点评 本题考查了物质性质的实验验证设计分析判断,性质试验的设计方法,掌握氮及其化合物的性质以及对装置流程的分析应用是解题关键,题目难度中等.

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案| A. | 明矾与水反应生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 当光束通过鸡蛋清水溶液时,能观察到丁达尔效应 | |
| C. | Li是最轻的金属,也是活动性较强的金属,是制造电池的理想物质 | |
| D. | 水泥厂用高压电作用于气溶胶以除去烟尘,是根据胶体带电这个性质而设计的 |
| A. | 缩小体积使压强增大 | B. | 体积不变充入稀有气体使压强增大 | ||
| C. | 体积不变充入He使压强增大 | D. | 压强不变充入稀有气体氖 |
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,用标准溶液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液由红色变为无色,且半分钟不再改变时,达到滴定终点.
(2)该小组在步骤①中的错误是锥形瓶不能用待测液润洗
由此造成的测定结果偏高(偏高、偏低或无影响)
(3)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)请根据下表数据计算待测烧碱溶液的浓度0.0800mol/L.
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前度数(mL) | 滴定后度数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
| A. | 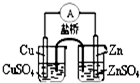 能组成Zn、Cu原电池 | B. |  能证明非金属性C>Si | ||
| C. | 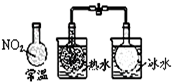 说明反应2NO2?N2O4△H>0 | D. | 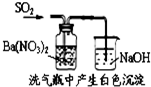 白色沉淀为BaSO4 |
 (3)镁离子Mg2+(4)硫离子
(3)镁离子Mg2+(4)硫离子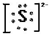 .
.