题目内容
16.下列各溶液中,微粒的物质的量浓度关系表述正确的是( )| A. | pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 | |
| B. | 常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 | |
| C. | 将0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 0.1 mol•L-1 Na2CO3溶液中:c(Na+)=c(HCO${\;}_{3}^{-}$)+c(H2CO3)+2c(CO${\;}_{3}^{2-}$) |
分析 A.氢氧化钡碱溶液抑制水的电离,碳酸钠是强碱弱酸盐,碳酸根离子水解促进水的电离;
B.醋酸是弱酸存在电离平衡,平衡状态下氢离子和氢氧化钠溶液中氢氧根离子恰好反应,醋酸又电离出氢离子,溶液显酸性;
C.溶液中存在电荷守恒;
D.碳酸钠溶液中在物料守恒n(Na)=2n(C),钠离子浓度等于碳元素所有存在形式离子的浓度总和.
解答 解:A.pH=12的Ba(OH)2溶液中水电离出的氢离子浓度=10-12mol/L,pH=12的Na2CO3溶液中碳酸根离子结合水电离出的氢离子分步水解,水电离出的氢离子浓度等于水电离出的氢氧根离子浓度=$\frac{1{0}^{14}}{1{0}^{-12}}$=10-2mol/L,水电离的c(H+)不相等,故A错误;
B.醋酸是弱酸,常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后,醋酸又电离出氢离子溶液显酸性,pH<7,故B正确;
C.将0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中为等浓度的NaA、NaCl、HA,溶液中存在电荷守恒c(Na+)+c(H+)=c(A-)+c(Cl-)+c(OH-),故C错误;
D.0.1 mol•L-1 Na2CO3溶液中存在物料守恒,:c(Na+)=2c(HCO3-)+2c(H2CO3)+2c(CO32-),故D错误,
故选B.
点评 本题考查了酸碱反应后溶液溶液酸碱性分析、弱电解质电离平衡、电荷守恒和好无聊守恒的分析应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.现有部分短周期主族元素的性质或原子结构如表:
(1)元素Y在周期表中的位置第二周期第ⅤA族(周期、族).
(2)XN2的电子式是: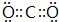 ,Y的简单氢化物的结构式
,Y的简单氢化物的结构式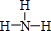 .
.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)用电子式表示WZ的形成过程 .
.
(5)元素Z和T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是B.
A.常温下Z单质和T单质状态不同B.Z的氢化物比T的氢化物稳定
C.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(6)写出W单质和H2O反应的化学方程式2Na+2H2O=2NaOH+H2↑所得溶液的溶质是离子化合物(填“离子”或“共价”).
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大的元素 |
| N | 原子序数比T小,且与T在同一主族 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氨化物的水溶液呈碱性 |
| Z | 元素最高正价为+7价 |
(2)XN2的电子式是:
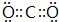 ,Y的简单氢化物的结构式
,Y的简单氢化物的结构式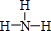 .
.(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)用电子式表示WZ的形成过程
 .
.(5)元素Z和T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是B.
A.常温下Z单质和T单质状态不同B.Z的氢化物比T的氢化物稳定
C.一定条件下,Z和T的单质都能与氢氧化钠溶液反应
(6)写出W单质和H2O反应的化学方程式2Na+2H2O=2NaOH+H2↑所得溶液的溶质是离子化合物(填“离子”或“共价”).
4.某溶液中的离子只有NH4+、Cl-、H+和OH-四种,下列描述正确的是( )
| A. | 该溶液中的溶质只有NH4Cl | |
| B. | 当溶液呈碱性时:c(NH4+)+c(H+)<c(Cl-)+c(OH-) | |
| C. | 溶液中离子浓度大小关系可能为:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 该溶液可能由pH=12的氨水与pH=2的HCl溶液等体积混合而成 |
11.下列说法正确的是( )
| A. | 浓度相同的NaNO3溶液和HNO3溶液中NO3-化学性质相同 | |
| B. | 等质量的红磷和白磷完全燃烧生成P2O5(s)放出热量相同 | |
| C. | 可以通过化学反应将淀粉转化为乙酸 | |
| D. | 同温下,等体积pH相同的NH4Cl溶液和HCl溶液中由水电离出的H+数目相同 |
5.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1 mol-NH2中含有的电子数为0.7NA | |
| B. | 标准状况下,2.24 L乙醇中含有的C-H数目为0.5NA | |
| C. | 常温常压下,65 g Zn与足量浓H2SO4充分反应,转移电子数一定为2NA | |
| D. | 2.24 L NO与1.12 L O2充分反应所得气体中原子数目一定为0.3NA |