题目内容
用惰性电极电解200mLCuSO4溶液.通电一段时间后,测定两极均产生224mL气体(已换算至标准状况下,且忽略溶液体积的变化及气体在溶液中的溶解),则原溶液中溶质的物质的量浓度和所得溶液的pH为( )
| A、0.04 mol?L-1 1 |
| B、0.02 mol?L-1 2 |
| C、0.03 mol?L-1 5 |
| D、0.05mol?L-1 1 |
考点:电解原理
专题:电化学专题
分析:电解CuSO4溶液质量增重的一极是电解池的阴极,析出铜,同时会产生氢气,电解方程式为:2CuSO4+2H20
2Cu+2H2SO4+O2↑,也可根据电解池两极上转移的电子数目相等计算,利用关系式为Cu~2e-~2H+来计算pH,根据电解方程式计算.
| ||
解答:
解:电解硫酸铜溶液,阳极上发生反应4OH--4e-═2H2O+O2↑,产生224mL即0.01mol气体,转移电子的物质的量是0.04mol,阴极上发生反应:Cu2++2e-═Cu,2H++2e-═H2↑,产生224mL即0.01mol气体,转移电子是0.02mol,所以反应:Cu2++2e-═Cu转移电子是0.02mol,铜离子的物质的量0.01mol,原溶液中溶质的物质的量浓度c=
=
=0.05mol?L-1,根据反应式:2CuSO4+2H20
2Cu+2H2SO4+O2↑,当生成0.01mol铜,生成硫酸是0.01mol,所以氢离子浓度是
=0.1mol/L,所以pH=1.
故选D.
| n |
| V |
| 0.01mol |
| 0.2L |
| ||
| 0.01mol×2 |
| 0.2L |
故选D.
点评:本题涉及电解原理的应用以及电极反应式的书写和电子守恒的计算知识,难度不大.

练习册系列答案
相关题目
有一在空气中暴露过的KOH固体,经分析测知含H2O3.12%,K2CO36%,其余为KOH.取此样品m g溶于100g 98%的硫酸里,残酸需加 n g KOH才刚好中和完全.由此可知蒸发中和后的溶液可得到多少克固体?( )
| A、14.2mg | ||
| B、174g | ||
C、
| ||
| D、无法计算 |
下列实验设计方案中,可行的是( )
| A、向某无色溶液中仅加入AgNO3溶液,以检验未知溶液中的Cl- | ||
| B、用洗气瓶中的NaOH溶液除去CO2气体中混有的HCl气体 | ||
C、向某无色溶液中仅加入BaCl2溶液,以检验未知溶液中的SO
| ||
| D、用加入适量铜粉的方法除去Cu(NO3)2溶液中的AgNO3杂质 |
在密闭容器中,对于反应2SO2(g)+O2(g)?2SO3(g),SO2和O2起始时分别为2.0mol和1.0mol;达平衡时,SO2的转化率为80%.若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起起始时SO3的物质的量及其转化率为( )
| A、1.0 mol和 10% |
| B、2.0 mol和 80% |
| C、2.0 mol和 40% |
| D、2.0 mol和 20% |
有13.6g氯化锌样品(其中混有另一种氯化物),将样品溶于水后加足量的硝酸银溶液,可得沉淀29.5g,则样品中可能含有下列哪一种氯化物( )
| A、氯化钾 | B、氯化汞 |
| C、氯化镁 | D、氯化钡 |
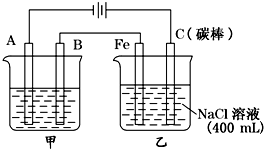 如图为相互串联的甲乙两电解池
如图为相互串联的甲乙两电解池 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应率的影响,在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应率的影响,在常温下按照如下方案完成实验.