题目内容
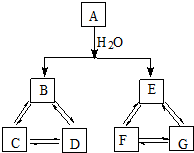 有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:
有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:(1)A、B、C、D含同一种元素;
(2)A、B、C、D、E、F、G都不是氧化物;
(3)D、G是钠盐;
(4)A、E、F、G含同一种元素,E在常温下为气体,且F为单质.
回答下列问题:
(1)写出A、F的化学式:A
(2)写出下列反应的离子方程式:
①D→C
②C+D→B
考点:无机物的推断
专题:推断题
分析:有A、B、C、D、E、F、G七种常见物质,都不是氧化物,A与水反应生成B与E,E在常温下为气体,应是发生水解反应,B为氢氧化物、E为氢化物,A、B、C、D含同一种元素,且D为钠盐,说明B能与氢氧化钠反应,可推知B为Al(OH)3,C为铝盐,D为NaAlO2,故A中含有Al元素;A、E、F、G含同一种元素,且F为单质、G是钠盐,E应为酸性气体,可推知E为H2S,F为S,G为Na2S,故A中含有S元素,综上分析可知A为Al2S3,验证符合转化关系,据此解答.
解答:
解:有A、B、C、D、E、F、G七种常见物质,都不是氧化物,A与水反应生成B与E,E在常温下为气体,应是发生水解反应,B为氢氧化物、E为氢化物,A、B、C、D含同一种元素,且D为钠盐,说明B能与氢氧化钠反应,可推知B为Al(OH)3,C为铝盐,D为NaAlO2,故A中含有Al元素;A、E、F、G含同一种元素,且F为单质、G是钠盐,E应为酸性气体,可推知E为H2S,F为S,G为Na2S,故A中含有S元素,综上分析可知A为Al2S3,验证符合转化关系,
(1)由上述分析可知,A为Al2S3,F的化学式为S,故答案为:Al2S3;S;
(2)反应①D→C是偏铝酸盐与酸反应转化为铝盐,反应离子方程式为:AlO2-+4H+═Al3++2H2O,
反应②C+D→B是铝盐、偏铝酸盐发生水解反应生成氢氧化铝沉淀,反应离子方程式为:3AlO2-+Al3++6H2O═4Al(OH)3↓,
故答案为:AlO2-+4H+═Al3++2H2O;3AlO2-+Al3++6H2O═4Al(OH)3↓.
(1)由上述分析可知,A为Al2S3,F的化学式为S,故答案为:Al2S3;S;
(2)反应①D→C是偏铝酸盐与酸反应转化为铝盐,反应离子方程式为:AlO2-+4H+═Al3++2H2O,
反应②C+D→B是铝盐、偏铝酸盐发生水解反应生成氢氧化铝沉淀,反应离子方程式为:3AlO2-+Al3++6H2O═4Al(OH)3↓,
故答案为:AlO2-+4H+═Al3++2H2O;3AlO2-+Al3++6H2O═4Al(OH)3↓.
点评:本题考查无机物推断,属于猜测验证型题目,没有明显的突破口,需要学生熟练掌握元素化合物性质,结合题目信息及转化关系进行猜测验证,对学生的推理有一定的要求,难度较大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列实验操作或事故处理中,做法不正确的是( )
| A、不慎将酸溅入眼中,立即用水冲洗,边洗边眨眼睛 |
| B、不慎将碱液沾到皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 |
| C、不慎碰翻酒精灯导致失火,马上用湿抹布扑灭 |
| D、稀释浓硫酸时,先把浓硫酸注入量筒,然后向其中加入水,边加边搅拌 |
能溶于水,能发生水解反应,还能发生银镜反应的是( )
| A、淀粉 | B、麦芽糖 |
| C、葡萄糖 | D、甲酸甲酯 |
 ,则该化合物的结构简式可能是(4种):
,则该化合物的结构简式可能是(4种): A、B、C是三种常见短周期元素的单质,常温下D为无色液体,E是一种常见的温室气体,F是化合物.其转化关系如图(反应条件和部分产物略去).
A、B、C是三种常见短周期元素的单质,常温下D为无色液体,E是一种常见的温室气体,F是化合物.其转化关系如图(反应条件和部分产物略去).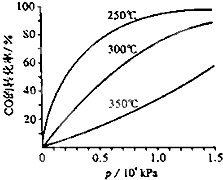 Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.