题目内容
14.下列关于胶体的叙述中正确的是( )| A. | 胶体是一种液态混合物,属于分散系的一种 | |
| B. | 用丁达尔效应可区分Fe(OH)3胶体、水、CuSO4溶液 | |
| C. | 用过滤器可以将胶体和溶液分开 | |
| D. | 胶体的本质特征是发生丁达尔效应 |
分析 A、液溶胶属于胶体的一种,是一种液态混合物,气溶胶为气体如空气,胶体不一定为液体,属于分散系的一种;
B.水、CuSO4溶液不具有丁达尔效应,颜色不同;
C.胶体和溶液都可以透过滤纸;
D.胶体的本质特征是分散质微粒直径介于1~100nm之间,不是发生丁达尔效应.
解答 解:A、液溶胶属于胶体的一种,是一种液态混合物,气溶胶为气体如空气,所以胶体不一定为液态,属于分散系的一种,故A错误;
B.用丁达尔效应可区分胶体和溶液,可以鉴别出Fe(OH)3胶体,水、CuSO4溶液利用颜色区别,故B正确;
C.胶体和溶液都可以透过滤纸,故过滤器不可以将胶体和溶液分开,故C错误;
D.胶体的本质特征是分散质微粒直径介于1~100nm之间,不是发生丁达尔效应,故D错误;
故选B.
点评 本题考查学生胶体的性质及应用、胶体本质和胶体与溶液的鉴别,可以根据所学知识进行回答,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列叙述中,正确的是( )
| A. | 所有主族中都有非金属元素 | |
| B. | 同周期元素中,ⅦA族元素的原子半径最大 | |
| C. | ⅥA族元素的原子,其半径越大,越容易得到电子 | |
| D. | 元素周期表中从ⅢB到ⅡB 10个纵列的元素都是金属元素 |
11.有机物甲的发光原理如下:
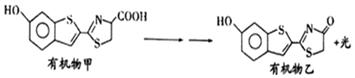
关于有机物甲和有机物乙的说法正确的是( )

关于有机物甲和有机物乙的说法正确的是( )
| A. | 互为同分异构体 | B. | 均可发生加成反应 | ||
| C. | 均可与碳酸氢钠溶液反应 | D. | 均最多有7个碳原子共平面 |
2.化学与生活息息相关.下列说法正确的是( )
| A. | 石英、水晶、水泥、光导纤维等物质的主要成分是SiO2 | |
| B. | 铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 医疗上,碳酸氢钠是治疗胃穿孔的一种药剂 | |
| D. | 肥皂水可用作蚊虫叮咬处的清洗剂 |
9.下列叙述正确的是( )
| A. | 金属氧化物不一定是碱性氧化物 | |
| B. | HC1、H2S、NH3都是电解质 | |
| C. | 强酸强碱都是离子化合物 | |
| D. | FeBr3、FeCl2、CuS都不能直接用化合反应制备 |
19.表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题.
(1)非金属性最强的元素是F(填元素符号,下同),形成化合物种类最多的元素是C.
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
(3)⑤⑥⑦单质的活泼性由强到弱的顺序为Na>Mg>Al (填元素符号),判断的实验依据是单质分别与水或酸反应的剧烈程度(或其最高价氧化物对应的水化物的碱性强弱) (写出一种).
(4)⑦、⑨的单质分别与⑤的最高价氧化物的水化物反应的离子方程式依次为2Al+2H2O+2OH-=2AlO2-+3H2↑、Cl2+2OH-=Cl-+ClO-+H2O.
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式,下同),具有两性的是Al(OH)3.
(3)⑤⑥⑦单质的活泼性由强到弱的顺序为Na>Mg>Al (填元素符号),判断的实验依据是单质分别与水或酸反应的剧烈程度(或其最高价氧化物对应的水化物的碱性强弱) (写出一种).
(4)⑦、⑨的单质分别与⑤的最高价氧化物的水化物反应的离子方程式依次为2Al+2H2O+2OH-=2AlO2-+3H2↑、Cl2+2OH-=Cl-+ClO-+H2O.
3.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(-57.3)kJ/mol | |
| B. | 500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℃、30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | CO(g)的燃烧热是283.0 kJ/mol,则表示CO燃烧热的热化学方程式为CO(g)+$\frac{1}{2}$O2(g)═CO2 (g)△H=-283.0 kJ/mol | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
4.将一块镁铝合金溶于盐酸后,加入过量氢氧化钠溶液,过滤后灼烧沉淀物,所得白色粉末的质量等于原合金的质量,则该合金中镁铝的质量比是( )
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 2:1 |
 ,D的简单气态氢化物的空间构型为三角锥形.
,D的简单气态氢化物的空间构型为三角锥形.