题目内容
下列各组元素中,电负性依次减小的是( )
| A、K、Na、Al |
| B、F、O、N |
| C、As、P、H |
| D、Se、S、O |
考点:元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:元素周期表中,元素得电子能力越大,其电负性越大,所以同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素,元素电负性随着原子序数增大而减弱,据此分析解答.
解答:
解:元素周期表中,元素得电子能力越大,其电负性越大,元素失电子能力越大,其电负性越小,所以同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素,元素电负性随着原子序数增大而减弱,
A.失电子能力大小顺序是K>Na>Al,所以电负性大小顺序是Al>Na>K,故A错误;
B.得电子能力顺序书写是F>O>N,所以电负性大小顺序是F>O>N,故B正确;
C.得电子能力大小顺序是P>As>H,所以电负性大小顺序是P>As>H,故C错误;
D.得电子能力大小顺序是O>S>Se,所以电负性大小顺序是O>S>Se,故D错误;
故选B.
A.失电子能力大小顺序是K>Na>Al,所以电负性大小顺序是Al>Na>K,故A错误;
B.得电子能力顺序书写是F>O>N,所以电负性大小顺序是F>O>N,故B正确;
C.得电子能力大小顺序是P>As>H,所以电负性大小顺序是P>As>H,故C错误;
D.得电子能力大小顺序是O>S>Se,所以电负性大小顺序是O>S>Se,故D错误;
故选B.
点评:本题考查电负性大小判断,明确元素得电子强弱与电负性大小关系是解本题关键,熟练掌握元素周期律并灵活运用,同时考查学生对基本理论的掌握,题目难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
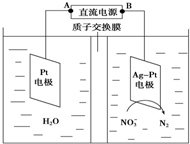 目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )
目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )| A、Pt电极为阴极 |
| B、电解过程中H+向正极移动 |
| C、理论上电解过程中阴、阳两极产生的气体在相同条件下体积比为2:5 |
| D、电解过程中Pt电极附近溶液的pH增大 |
可以用来鉴别Cl-、Br-、I-离子的是( )
| A、AgNO3溶液和稀硝酸 |
| B、观察它们的颜色 |
| C、用焰色反应进行实验 |
| D、分别向里滴加氯水 |
食盐、食醋、纯碱均为家庭厨房中常用的物质.利用这些物质不能完成的实验是( )
| A、鉴别食盐和纯碱 |
| B、验证蛋壳的主要成分为CaCO3 |
| C、除去热水瓶内壁上的水垢 |
| D、检验自来水中是否含有Cl- |
“厨房化学”是指利用家庭生活用品来进行化学实验,从而对化学进行学习和探究的活动.下列实验在厨房中不能完成的是( )
| A、检验鸡蛋壳中含有碳酸盐 |
| B、检验蛋白质在加热条件下能发生变性 |
| C、检验加碘食盐中不含碘单质 |
| D、检验自来水中含有Cl-离子 |
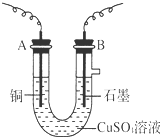 某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)
某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示) 某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究.
某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究.