题目内容
15.氯气溶于水达到平衡后,若只改变某一条件,下列叙述正确的是( )| A. | 通入少量SO2,溶液漂白性增强 | |
| B. | 加入少量NaHCO3固体,c(ClO)减小 | |
| C. | 加入少量水,水的电离平衡向正方向移动 | |
| D. | 加入NaOH固体至恰好完全反应,一定有c(Na+)=c(Cl-)+c(ClO-)+c(HClO) |
分析 A.通入二氧化硫,其与氯气反应生成无漂白性的盐酸和硫酸,平衡左移,漂白性减弱;
B.氯气与水反应后溶液中的盐酸可以和碳酸氢钠反应,促进平衡正向移动,据此回答;
C.氯气与水的反应,加入水,电离平衡向右移动;
D.根据物料守恒结合溶液的组成来回答.
解答 解:在氯水中存在如下平衡:Cl2+H2O?HCl+HClO、H2O?H++OH-、HClO?H++ClO-.
A.通入少量SO2,发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,平衡左移,HClO的浓度减小,溶液漂白性减弱,故A错误;
B.入少量NaHCO3固体,消耗盐酸,此时平衡正向移动,所以c(ClO-)增加,故B错误;
C.加入少量水,Cl2+H2O?HCl+HClO正向移动,促进水的电离,水的电离平衡向正反应方向移动,故C正确;
D.加入少量固体氢氧化钠,溶液中存在氯化钠、次氯酸钠的混合物,则有:c(H+)<c(OH-),存在物料守恒:c(Na+)=c(Cl-)+c(ClO-)+c(HClO)故C正确;
故选CD.
点评 本题考查了电离平衡和化学平衡,注意氯气溶于水达到平衡时,该溶液为饱和溶液,易错选项是A,注意次氯酸和二氧化硫都有漂白性,但二者因发生氧化还原反应而导致二者混合时消失漂白性,为易错点.

练习册系列答案
相关题目
5.下列化学用语表示不正确的是( )
| A. | 钠离子的结构示意图: | |
| B. | 原子核内有20个中子的氯原子:${\;}_{17}^{37}$Cl | |
| C. | 氢氧根离子的电子式: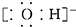 | |
| D. | NaHCO3的电离方程式:NaHCO3=Na++H++CO32- |
3.下列不适合添加在药皂中的是( )
| A. | 硫磺 | B. | 苯酚 | C. | 硼酸 | D. | 甲醛 |
10.如图所示下列分析错误的是( )


| A. | 只闭合K2,该装置将电能转化为化学能 | |
| B. | 只闭合K1,石墨棒周围溶液pH逐渐升高 | |
| C. | 只闭合K2,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 | |
| D. | 铁腐蚀的速度由大到小的顺序是:只闭合K1>都断开>只闭合K2 |

 )的合成路线如下:
)的合成路线如下: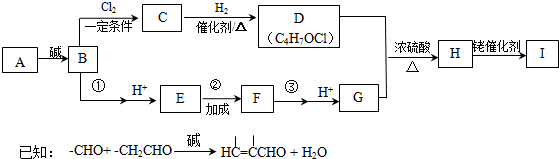
 ,B→C的反应类型为取代反应.
,B→C的反应类型为取代反应. .
.
 .
. .
. 的合成路线(无机原料任选).
的合成路线(无机原料任选). H2SO3; H2SO3
H2SO3; H2SO3  H++HSO3-;HSO3-
H++HSO3-;HSO3-  H++SO32-.
H++SO32-.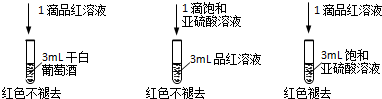
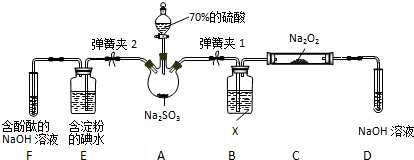
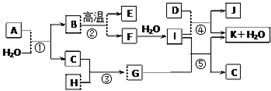 如图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出.已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于泳池消毒.反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法.
如图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出.已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于泳池消毒.反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法. ;I中所含化学键类型离子键、共价键.
;I中所含化学键类型离子键、共价键.