题目内容
反应2SO2+O2
2SO3+Q达到化学平衡状态时的标志是( )
| 催化剂 |
| A、SO2的消耗速率等于SO3的生成速率 |
| B、SO2的生成速率等于SO3的生成速率 |
| C、SO2的消耗速率大于O2生成速率的2倍 |
| D、SO3的生成速率等于O2的生成速率 |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、SO2的消耗速率等于SO3的生成速率,都体现的正反应方向,故A错误;
B、SO2的生成速率等等效于SO3的消耗速率等于SO3的生成速率说明达平衡状态,故B正确;
C、SO2的消耗速率应等于O2生成速率的2倍,故C错误;
D、SO3的生成速率等于O2的生成速率,速率之比不等于对应物质的计量数之比,故D错误;
故选B.
B、SO2的生成速率等等效于SO3的消耗速率等于SO3的生成速率说明达平衡状态,故B正确;
C、SO2的消耗速率应等于O2生成速率的2倍,故C错误;
D、SO3的生成速率等于O2的生成速率,速率之比不等于对应物质的计量数之比,故D错误;
故选B.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
常温下,下列溶液pH小于7的是( )
| A、CH3COONa |
| B、CuSO4 |
| C、NaOH |
| D、Na2CO3 |
PH=3的盐酸和醋酸各100mL,分别和锌反应,反应完后,放出的气体一样多.若最后有一溶液中锌剩余,则下列判断正确的是( )
| A、反应开始时速率v(HCl)>v(CH3COOH) |
| B、加入的锌质量相等 |
| C、盐酸中锌有剩余 |
| D、反应开始后不久,醋酸反应的速率小于盐酸 |
下列物质属于弱电解质的是( )
| A、氯化钠 | B、蔗糖 | C、醋酸 | D、硫酸 |
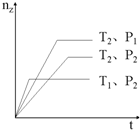 反应aX(g)+bY(g)cZ(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应aX(g)+bY(g)cZ(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是( )| A、T1<T2,P1<P2,a+b<c正反应是吸热反应 |
| B、T1<T2,P1>P2,a+b<c正反应是吸热反应 |
| C、T1>T2,P1>P2,a+b>c逆反应是吸热反应 |
| D、T1>T2,P1<P2,a+b>c逆反应是吸热反应 |
氯气跟氢氧化钠溶液反应:Cl2+2NaOH→NaClO+NaCl+H2O,下列叙述中不正确的是( )
| A、氯气既是氧化剂,又是还原剂 |
| B、次氯酸钠是氧化产物,氯化钠是还原产物 |
| C、氢氧化钠既不是氧化剂,也不是还原剂 |
| D、电子的转移数是2,从氯气转移到氢氧化钠 |
主族元素X、Y、Z的离子的电子层结构相同,原子半径X>Z,离子半径Y>X,Y和Z能形成离子化合物,由此可判断三种元素的原子序数是( )
| A、X>Y>Z |
| B、Z>Y>X |
| C、Y>X>Z |
| D、X>Z>Y |
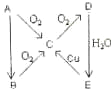 A、B、C、D、E、在一定条件下的转换条件如图所示:
A、B、C、D、E、在一定条件下的转换条件如图所示: