题目内容
下列分子结构中,所有原子不能都满足最外层为8电子稳定结构的是( )
| A、CO2 |
| B、H2O |
| C、N2 |
| D、CCl4 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:根据原子最外层电子数和化合价判断,在共价化合物中,原子最外层电子数等于原子的价层电子数+|化合价|,以此进行分析.
解答:
解:A、CO2中,C原子的最外层电子为:4+4=8,O原子的最外层电子为:6+|-2|=8,都满足8电子稳定结构,故A错误;
B、H2O中,O原子的最外层电子数为6+2=8,H原子的最外层电子数为1+1=2,不满足8电子稳定结构,故B正确;
C、N2中,电子式为 ,满足8电子稳定结构,故C错误;
,满足8电子稳定结构,故C错误;
D、CCl4中,C原子的最外层电子为:4+4=8,Cl原子的最外层电子为:7+|-1|=8,都满足8电子稳定结构,故D错误;
故选B.
B、H2O中,O原子的最外层电子数为6+2=8,H原子的最外层电子数为1+1=2,不满足8电子稳定结构,故B正确;
C、N2中,电子式为
 ,满足8电子稳定结构,故C错误;
,满足8电子稳定结构,故C错误;D、CCl4中,C原子的最外层电子为:4+4=8,Cl原子的最外层电子为:7+|-1|=8,都满足8电子稳定结构,故D错误;
故选B.
点评:本题考查原子核外电子是否满足8电子稳定结构,题目难度不大,注意判断问题的角度及H原子的特殊情况.

练习册系列答案
相关题目
某原子的最外层电子排布为nsnnp2n+1,则该元素在周期表中的位置为( )
| A、第二周期,ⅢA族 |
| B、第二周期,ⅦA族 |
| C、第五周期,ⅡA族 |
| D、第七周期,ⅡA族 |
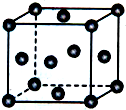 已知X、Y、Z为短周期元素,X、Y同周期,X和Z同主族,Y原子基态时2p轨道上的未成对电子数最多,X的低价氧化物和Y单质分子的电子数相等.W2+的核外电子排布简式为[Ar]3d9.
已知X、Y、Z为短周期元素,X、Y同周期,X和Z同主族,Y原子基态时2p轨道上的未成对电子数最多,X的低价氧化物和Y单质分子的电子数相等.W2+的核外电子排布简式为[Ar]3d9.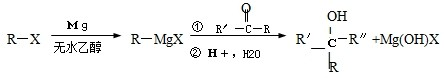
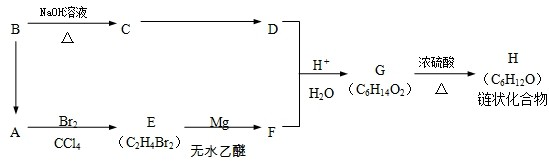
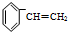 )聚合而成,是一种多功能塑料,广泛应用于食品包装,机器设备等许多日常生活领域中.写出以D和苯为主要原料制备苯乙烯(
)聚合而成,是一种多功能塑料,广泛应用于食品包装,机器设备等许多日常生活领域中.写出以D和苯为主要原料制备苯乙烯(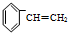 )的合成路线流程图,无机试剂任选.(合成路线常用表示方法为:A
)的合成路线流程图,无机试剂任选.(合成路线常用表示方法为:A
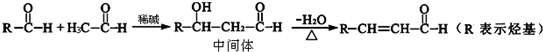
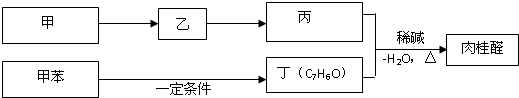
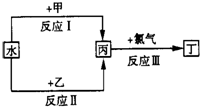
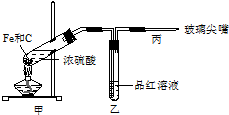 (1)下列仪器在使用前必须检查其是否漏水的是
(1)下列仪器在使用前必须检查其是否漏水的是