题目内容
2.下列说法正确的是( )| A. | 相同温度下,0.6mol/L氨水溶液与0.3mol/L氨水溶液中c(OH-)之比是2:1 | |
| B. | 将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)>c(NH4+) | |
| C. | 25℃时,10mL 0.02mol•L-1HCl溶液与10mL0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12 | |
| D. | 25℃时pH=10的NaOH溶液与60℃时pH=10的NaClO溶液中:c(H+)相等 |
分析 A.氨水的浓度不同时,一水合氨的电离程度不同;
B.溶液pH=7时,c(OH-)=c(H+),结合电荷守恒分析硫酸根离子与铵根离子浓度关系;
C.下计算出混合液中氢氧根离子浓度,pH=12的溶液中氢氧根离子浓度为0.01mol/L;
D.根据pH=-lgc(H+)可知,两溶液中氢离子浓度都是1×10-10mol/L.
解答 解:A.相同温度下,0.6mol/L氨水溶液与0.3mol/L氨水溶液中,由于一水合氨的电离程度不同,则两溶液中c(OH-)之比不是2:1,故A错误;
B.溶液的pH=7,呈中性,则c(OH-)=c(H+),结合电荷守恒可知:2c(SO42-)=c(NH4+),故B错误;
C.常温下pH=12的溶液中氢氧根离子浓度为0.01mol/L,10mL 0.02mol•L-1HCl溶液与10mL0.02mol•L-1Ba(OH)2溶液充分混合,混合液中氢氧根离子浓度为:$\frac{0.02mol/L×2×0.01L-0.02mol/L}{0.02L}$=0.005mol/L≠0.01mol/L,则混合液的pH≠12,故C错误;
D.25℃时pH=10的NaOH溶液与60℃时pH=10的NaClO溶液中:c(H+)=10-pH=1×10-10mol/L,两溶液中氢离子浓度相等,故D正确;
故选D.
点评 本题考查了弱电解质电离平衡、离子浓度大小比较及溶液pH的计算等知识,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电荷守恒的含义及应用方法,试题培养了学生的灵活应用能力.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
12.如图所示,甲装置可直接除去城市废水中的尿素,既能产生净化的水,又能发电.乙装置可用于人工肾脏间接电化学方法除去代谢产物中的尿素的工作原理.

下列关于描述正确的是( )

下列关于描述正确的是( )
| A. | 甲乙装置连接是a接c、b接d | |
| B. | 甲装置工作时H+ 移向负极 | |
| C. | 乙装置阴极室溶液的pH与电解前相比将升高 | |
| D. | a和c电极都发生CO(NH2)2-6e-+H2O═N2↑+CO2↑+6H+ |
10.下列叙述正确的是( )
| A. | 同周期元素的原子半径以ⅤⅡA族的为最大 | |
| B. | 同主族元素两种元素原子的核外电子数的差值可能为26 | |
| C. | 短周期元素中次外层电子数是最外层电子数2倍的原子一定是非金属元素 | |
| D. | 同周期第ⅡA族和ⅢA族元素的原子序数之差不可能为25 |
17.据环保部门测定,我国一些大城市的酸雨pH=3.5.在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是( )
| A. | Fe-2e-═Fe2+ | B. | 2H2O+O2+4e-═4OH- | ||
| C. | 2H++2e-═H2↑ | D. | 4OH--4e-═2H2O+O2↑ |
2.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 7.2g CaO2晶体中阴离子和阳离子总数为0.3NA | |
| B. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol放出热量9.2kJ时,转移电子0.6NA | |
| C. | 0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1NA | |
| D. | 0.1 mol H2O2分子中含极性共价键数目为0.3NA |
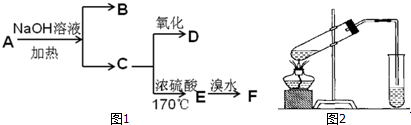
 ,反应类型氧化反应;
,反应类型氧化反应; ,反应类型加聚反应.
,反应类型加聚反应.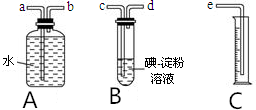 某化学兴趣小组选用如图实验装置,测定某工业尾气(含SO2、N2、O2)中SO2的含量.
某化学兴趣小组选用如图实验装置,测定某工业尾气(含SO2、N2、O2)中SO2的含量.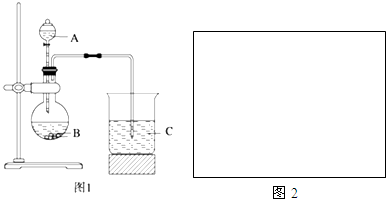
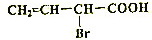 ,试回答:
,试回答: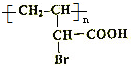 ;
;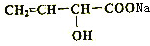 +NaBr+H2O;
+NaBr+H2O;