题目内容
20.有机化合物香醇可以用作食用香精,其结构如图所示: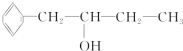
(1)香醇的分子式为C10H14O;它可能发生的有机反应类型是①②③⑤(填序号).
①取代反应 ②加成反应 ③消去反应 ④聚合反应 ⑤氧化反应 ⑥水解反应
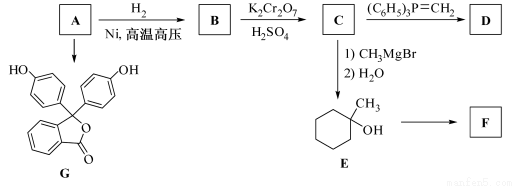
(2)有机物丙(C13H18O2)是一种香料,其合成路线如图所示,其中甲的相对分子质量为88,它的核磁共振氢谱中有3组峰,乙为香醇的同系物.
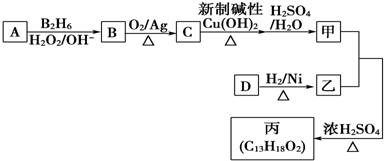
已知:R-CH═CH2$→_{H_{2}O_{2}/OH-}^{B_{2}H_{6}}$R-CH2CH2OH,请回答下列问题:
①A的系统命名名称为2-甲基丙烯;
②写出C与新制Cu(OH)2悬浊液反应的化学方程式:(CH3)2CHCHO+2Cu(OH)2 $\stackrel{△}{→}$(CH3)2CHCOOH+Cu2O↓+2H2O;
③丙分子中有两个甲基,在一定条件下,1mol D可以和2mol H2反应生成乙,D可以发生银镜反应,则D的结构简式为
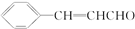 ;
;④甲与乙反应的化学方程式为
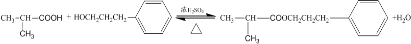 ;
;⑤甲的同分异构体中含有“-COO-”结构的共有5种.
分析 (1)根据香醇的结构简式书写其分子式;由结构可知,可以醇羟基,具有醇的性质,含有苯环,具有苯的性质;
(2)A发生信息反应生成B,B连续氧化、酸化得到甲,则甲为羧酸,相对分子质量为88,减去1个-COOH后剩余基团的式量=88-45-43,为-C3H7,它的核磁共振氢谱显示只有三组峰,则甲为2-甲基丙酸,结合转化关系可知,A为2-甲基丙烯,结构简式为CH2=C(CH3)2,B为2-甲基-1-丙醇,结构简式为(CH3)2CHCH2OH,C为2-甲基丙醛,结构简式为:(CH3)2CHCHO,甲与乙反应酯化生成丙(C13H18O2),则乙为C9H12O,丙中有两个甲基,则乙中不含甲基,乙为香醇的同系物,则乙的结构简式为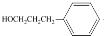 ,由1molD与2mol氢气反应生成乙,所以D为C9H8O,可以发生银镜反应,含有-CHO,故D为
,由1molD与2mol氢气反应生成乙,所以D为C9H8O,可以发生银镜反应,含有-CHO,故D为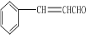 ,然后结合物质的结构与性质来解答.
,然后结合物质的结构与性质来解答.
解答 解:(1)由香醇的结构可知,其分子式为C10H14O,含有醇羟基,可以发生氧化、取代、消去反应,含有苯环,含有发生加成反应,不能发生水解、聚合反应,
故答案为:C10H14O;①②③⑤;
(2)A发生信息反应生成B,B连续氧化、酸化得到甲,则甲为羧酸,相对分子质量为88,减去1个-COOH后剩余基团的式量=88-45-43,为-C3H7,它的核磁共振氢谱显示只有三组峰,则甲为2-甲基丙酸,结合转化关系可知,A为2-甲基丙烯,结构简式为CH2=C(CH3)2,B为2-甲基-1-丙醇,结构简式为(CH3)2CHCH2OH,C为2-甲基丙醛,结构简式为:(CH3)2CHCHO.甲与乙反应酯化生成丙(C13H18O2),则乙为C9H12O,丙中有两个甲基,则乙中不含甲基,乙为香醇的同系物,则乙的结构简式为 ,由1molD与2mol氢气反应生成乙,所以D为C9H8O,可以发生银镜反应,含有-CHO,故D为
,由1molD与2mol氢气反应生成乙,所以D为C9H8O,可以发生银镜反应,含有-CHO,故D为 ,
,
①由上述分析可知,A为2-甲基丙烯,故答案为:2-甲基丙烯;
②C与新制Cu(OH)2悬浊液反应的化学方程式为(CH3)2CHCHO+2Cu(OH)2 $\stackrel{△}{→}$(CH3)2CHCOOH+Cu2O↓+2H2O,
故答案为:(CH3)2CHCHO+2Cu(OH)2 $\stackrel{△}{→}$(CH3)2CHCOOH+Cu2O↓+2H2O;
③由上述分析可知,D的结构简式为 ,故答案为:
,故答案为: ;
;
④甲与乙反应的化学方程式为 ,
,
故答案为: ;
;
⑤甲为2-甲基丙酸,甲的同分异构体中含有“-COO-”,属于酯或羧酸的结构,
构成酯的酸、与醇有以下情况:
酸为丙酸、醇为甲醇,有1种,
酸为乙酸、醇为乙醇,有1种,
酸为甲酸、醇为丙醇,丙醇有2种,故形成的酯有2种,
如果属于羧酸,为丁酸,
故符合条件的甲的同分异构体有5种,
故答案为:5.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析判断及获取信息运用信息解答问题能力,根据反应条件、某些物质分子式、题给信息进行解答,甲的相对分子质量利用残余法确定其结构是解题的关键,易错点是同分异构体种类判断.

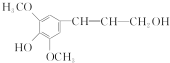
| A. | 芥子醇的分子式为C11H14O4 | |
| B. | 芥子醇分子中所有碳原子可能在同一平面上 | |
| C. | 1 mol该化合物在一定条件下最多可与2molNaOH反应 | |
| D. | 芥子醇在一定条件下能发生氧化、取代、加成、酯化反应 |
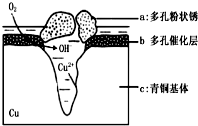 青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法不正确的是( )
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法不正确的是( )| A. | 腐蚀过程中,负极 b 被氧化 | |
| B. | 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓ | |
| C. | 若生成 2.145gCu 2 ( OH ) 3 Cl,则理论上消耗标准状况氧气体积为 0.448L | |
| D. | 正极的电极反应式为:正极反应是 O2+4e-+2H2O=4OH- |
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
 在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )
在一定温度下,将1mol X气体和1mol Y气体充入2L密闭容器中,发生如下反应:X(g)+Y(g)?aZ(g)+W(s)△H>0,t1时刻达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体Z的浓度随时间的变化如下图所示,下列说法正确的是( )| A. | 该反应在0~t1时间段的速率为:ν(W)=0.25/t1 mol•L-1•min-1 | |
| B. | 反应方程式中的a不可能等于1 | |
| C. | t2时刻改变的条件是通入少量气体Z | |
| D. | t3时刻改变的条件是移去少量物质W |
 某研究性学习小组用PH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的PH值(选用酚酞作为指示剂)
某研究性学习小组用PH=1的盐酸滴定25.00mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的PH值(选用酚酞作为指示剂)①实验过程中需要使用的仪器有铁架台、滴定管夹、碱式滴定管、胶头滴管、酸式滴定管、锥形瓶,
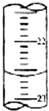
②如图,是某次滴定时的滴定管中的液面,其读数为22.60mL.
③如何判断滴定到达终点当滴加最后一滴盐酸,溶液的颜色由黄色变为橙色,且在半分钟内不变色.
③根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:BD.
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用盐酸溶液润洗
C、锥形瓶水洗后未干燥
D、酸式滴定管尖嘴部分有气泡,滴定后消失.
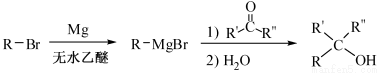
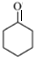
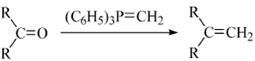 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢) 、
、
 或
或 (任写一种)
(任写一种)
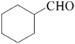 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
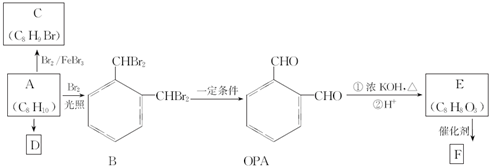
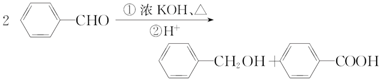
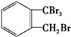 .
.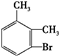 、
、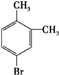 .
.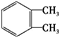 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$ $→_{△}^{CH_{3}CH_{2}OH、浓硫酸}$
$→_{△}^{CH_{3}CH_{2}OH、浓硫酸}$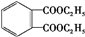 .
.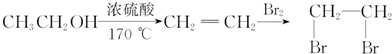
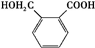 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$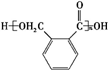 +(n-1)H2O.
+(n-1)H2O. .
.