题目内容
把一定量的有机物溶于NaOH溶液中,滴入酚酞试液呈红色,煮沸5分钟后,溶液颜色变浅,再加入盐酸,显酸性析出白色晶体,取少量晶体放到FeCl3溶液中,溶液呈紫色,则有机物可能是下列物质中的( )
A、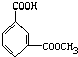 |
B、 |
C、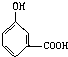 |
D、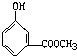 |
考点:烃的衍生物官能团,有机物分子中的官能团及其结构
专题:有机反应
分析:取少量晶体放在FeCl3溶液中,溶液呈现紫色,说明有机物中含有酚羟基,煮沸5min后溶液颜色变浅,说明有机物中含有在碱性条件下水解的官能团,以此解答该题.
解答:
解:有机物溶解于适量的NaOH溶液中,滴入酚酞试液呈红色,有机物有弱酸性,则含有酚羟基,煮沸5min后,溶液颜色变浅,再加入盐酸显酸性后,沉淀出白色晶体;取少量晶体放到FeCl3溶液中,溶液又呈紫色,该有机物含有苯酚酯的结构,选项中只有D选项符合含有酚羟基、苯酚酯的结构,
故选D.
故选D.
点评:本题考查有机物的结构与性质,明确苯酚和酯的性质是解答本题的关键,注意苯酚的显色反应,题目难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某硬水中钙、镁离子均以氯化物的形式存在,可用石灰纯碱法将其软化.具体步骤是:先加入石灰将水中的镁离子沉淀,再加入纯碱使水中的钙离子沉淀.发生反应的离子方程式正确的是( )
| A、Ca(OH)2+Mg2+=Mg(OH)2+Ca2+ |
| B、2OH-+Mg2+=Mg(OH)2↓ |
| C、Na2CO3+Ca2+=CaCO3↓+2Na+ |
| D、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法是( )
| A、加入适量的NaBr溶液 |
| B、通入溴蒸气 |
| C、加入适量的NaOH溶液 |
| D、加适量的KI溶液 |
用NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A、标准状总下11.2L臭氧中含有1.5NA个氧原子 |
| B、NO2与N2O4混合气体46g含有的原了总数为3NA |
| C、1molMg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
| D、100mL 0.2mol?L-1稀硫酸中含有硫酸根的个数为0.2NA |
下列说法正确的是( )
| A、能使品红褪色的不一定是SO2 |
| B、因为SO2有漂白性,所以它能使品红溶液、溴水、高锰酸钾褪色 |
| C、漂白粉、SO2、Na2O2、活性炭都使能红墨水褪色,其原理相同 |
| D、为了增强漂白性,将SO2和Cl2这两种气体同时作用于潮湿的有色布条使其褪色 |
 向纯醋酸加水,溶液的导电能力随着加入水的量的变化如图所示:
向纯醋酸加水,溶液的导电能力随着加入水的量的变化如图所示: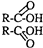
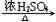
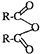 +H2O
+H2O