题目内容
2012年6月,神九与天宫一号成功的实现了自动对接和手动对接,标志着我国的航天事业又取得了新进展.火箭推进器中常用强还原剂N2H4(l)和强氧化剂H2O2(l),当它们混合反应时,即产生大量的N2(g)和H2O(g),并放出大量热,已知0.4mol N2H4(l)和0.8molH2O2(l)反应生成N2(g)和H2O(g)时,放出256.7kJ热量.
(1)写出该反应的热化学方程式. .
(2)16g N2H4(l)与足量H2O2(l)反应生成N2(g)和H2O(g)时,放出的热量为 kJ.
(1)写出该反应的热化学方程式.
(2)16g N2H4(l)与足量H2O2(l)反应生成N2(g)和H2O(g)时,放出的热量为
考点:热化学方程式
专题:化学反应中的能量变化
分析:(1)根据0.4mol液态肼放出的热量,计算1mol液态肼放出的热量,然后根据热化学方程式的书写方法写出热化学方程式;
(2)先根据质量求出物质的量,在根据物质的量之比等于热量比求算.
(2)先根据质量求出物质的量,在根据物质的量之比等于热量比求算.
解答:
解:(1)0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为
=614.8kJ,所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-614.8kJ/mol,
故答案为:N2H4 (l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.8kJ?mol-1;
(2))16g N2H4(l)与足量H2O2(l)反应生成N2(g)和H2O(g),则c(N2H4)=
=
=0.5mol,
则
=
,解得Q=320.9kJ;
故答案为:320.9kJ.
| 256.7kJ |
| 0.4 |
故答案为:N2H4 (l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.8kJ?mol-1;
(2))16g N2H4(l)与足量H2O2(l)反应生成N2(g)和H2O(g),则c(N2H4)=
| m |
| M |
| 16g |
| 32g/mol |
则
| 1mol |
| 0.5mol |
| 614.8KJ |
| Q |
故答案为:320.9kJ.
点评:本题考查了热化学方程式的书写方法和注意问题及反应热的计算,题目难度不大,侧重于基础知识的考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各装置中,能够成原电池的是( )
A、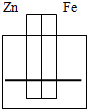 乙醇 |
B、 稀硫酸 |
C、 稀硫酸 |
D、 稀硫酸 稀硫酸 |
 下列反应前后物质的总能量变化可用如图表示的是( )
下列反应前后物质的总能量变化可用如图表示的是( )| A、石灰石在高温下的分解反应 |
| B、生石灰和水的反应 |
| C、盐酸与氢氧化钠溶液的反应 |
| D、木炭在氧气中燃烧 |
下列离子方程式书写正确的是( )
| A、少量的金属铜投入浓硝酸中Cu+4H++2NO3-=Cu2++NO2↑+2H2O |
| B、铝片投入稀盐酸中Al+6H+=Al3++3H2↑ |
| C、氢氧化钡溶液与稀硫酸混合Ba2++SO42-=BaSO4↓ |
| D、氢氧化铝与足量烧碱溶液混合Al(OH)3+OH-=AlO2-+2H2O |

 ,比较它们的电子层数和核电荷数,按照Na、Mg、Al顺序排布,试解释它们金属性逐渐减弱的原因.
,比较它们的电子层数和核电荷数,按照Na、Mg、Al顺序排布,试解释它们金属性逐渐减弱的原因.