题目内容
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol FeCl3完全水解生成NA个胶体粒子 |
| B、常温常压下,23g NO2分子总数小于0.5NA |
| C、标准状况下,2.24 L的CCl4中含有的C-Cl键数为0.4NA |
| D、6.8g熔融态KHSO4中含有0.1NA个阳离子 |
考点:阿伏加德罗常数
专题:
分析:A、氢氧化铁胶体微粒是氢氧化铁微粒的集合体;
B、在NO2气体中存在平衡:2NO2?N2O4;
C、标况下,四氯化碳为液态;
D、熔融状态下的硫酸氢钾只能电离为K+和HSO4-,6.8g硫酸氢钾的物质的量为0.05mol,含有0.05mol钾离子.
B、在NO2气体中存在平衡:2NO2?N2O4;
C、标况下,四氯化碳为液态;
D、熔融状态下的硫酸氢钾只能电离为K+和HSO4-,6.8g硫酸氢钾的物质的量为0.05mol,含有0.05mol钾离子.
解答:
解:A、胶体粒子是氢氧化铁的集合体,所以胶体粒子小于NA个,故A错误;
B、23gNO2的物质的量为0.5mol,大在NO2气体中存在平衡:2NO2?N2O4会导致气体的物质的量减小,故分子数目小于0.5NA,故B正确;
C、标况下,四氯化碳为液态,故C错误;
D.6.8g熔融KHSO4的物质的量为0.05mol,熔融状态下的硫酸氢钾只能电离为K+和HSO4-,所以0.05mol硫酸氢钾中含有0.05mol阳离子,含有0.05NA个阳离子,故D错误;
故选B.
B、23gNO2的物质的量为0.5mol,大在NO2气体中存在平衡:2NO2?N2O4会导致气体的物质的量减小,故分子数目小于0.5NA,故B正确;
C、标况下,四氯化碳为液态,故C错误;
D.6.8g熔融KHSO4的物质的量为0.05mol,熔融状态下的硫酸氢钾只能电离为K+和HSO4-,所以0.05mol硫酸氢钾中含有0.05mol阳离子,含有0.05NA个阳离子,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列溶液中含3种分子的是( )
| A、氯水 | B、溴的四氯化碳溶液 |
| C、醋酸溶液 | D、酒精水溶液 |
用足量的碳粉还原1mol金属氧化物,经充分反应生成的CO和CO2在标准状况下共40.32L,该金属氧化物可能是( )
| A、CuO |
| B、Fe3O4 |
| C、Al2O3 |
| D、PbO2 |
下列反应属于氧化还原反应的是( )
| A、14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4 | ||||
B、MgCl2(熔融)
| ||||
| C、CaCO3+2HCl═CaCl2+CO2↑+H2O | ||||
| D、Na2O+H2O═2NaOH |
某反应过程能量变化如图所示,下列说法正确的是( )
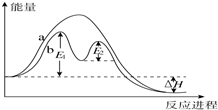

| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应不等于△H |
| C、使用催化剂,可改变该反应的活化能 |
| D、有催化剂条件下,反应的活化能等于E1-E2 |
已知某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能存在的离子组是( )
| A、Al3+、CH3COO-、Cl- |
| B、Mg2+、Ba2+、Br- |
| C、MnO4-、Na+、I-、 |
| D、Na+、NH4+、Cl- |
下列表示对应化学反应的离子方程式正确的是( )
A、向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-
| ||||
| B、用白醋除铁锈:Fe2O3+6H+═3H2O+2Fe3+ | ||||
| C、次氯酸钠溶液中通入过量二氧化硫:ClO-+H2O+SO2=HClO+HSO3- | ||||
D、用惰性电极电解饱和MgCl2溶液:2Cl-+2H2O
|