题目内容
已知氢元素和氧元素能形成以下4种微粒:H2O、H2O2、OH-、H3O+.
(1)写出氧的原子结构示意图: 用AZX表示法写出质量数为2的氢原子:
(2)以上4种微粒,电子数与其他三种不同的是:
(3)现有10g由1H和18O组成的水分子,其中含质子数 mol,含中子数 个.
(1)写出氧的原子结构示意图:
(2)以上4种微粒,电子数与其他三种不同的是:
(3)现有10g由1H和18O组成的水分子,其中含质子数
考点:原子结构与元素的性质,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:(1)氧原子核外有8个电子,分2层排布;质量数为2的氢原子,质子数为1;
(2)根据分子的电子数等于各原子的电子数之和,阳离子的电子数等于各原子的电子数之和减去电荷数,阴离子的电子数等于各原子的电子数之和加上电荷数;
(3)根据n=
结合原子构成计算.
(2)根据分子的电子数等于各原子的电子数之和,阳离子的电子数等于各原子的电子数之和减去电荷数,阴离子的电子数等于各原子的电子数之和加上电荷数;
(3)根据n=
| m |
| M |
解答:
解:(1)氧原子核外有8个电子,分2层排布,则氧的原子结构示意图: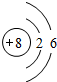 ;质量数为2的氢原子,质子数为1,该氢原子表示为:
;质量数为2的氢原子,质子数为1,该氢原子表示为:
H;
故答案为: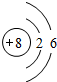 ;
;
H;
(2)H2O含有10个电子,H2O2含有18个电子,OH-含有10个电子,H3O+含有10个电子,所以电子数与其他三种不同的是:H2O2;
故答案为:H2O2;
(3)10g由1H和18O组成的水分子,其物质的量为n=
=
=0.5mol,一个由1H和18O组成的水分子含有10个质子,则含有的质子的物质的量为0.5mol×10=5mol,一个由1H和18O组成的水分子含有10个中子,则0.5mol水中中子数为5NA;
故答案为:5;5NA.
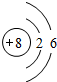 ;质量数为2的氢原子,质子数为1,该氢原子表示为:
;质量数为2的氢原子,质子数为1,该氢原子表示为:2 1 |
故答案为:
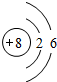 ;
;2 1 |
(2)H2O含有10个电子,H2O2含有18个电子,OH-含有10个电子,H3O+含有10个电子,所以电子数与其他三种不同的是:H2O2;
故答案为:H2O2;
(3)10g由1H和18O组成的水分子,其物质的量为n=
| m |
| M |
| 10g |
| 20g/mol |
故答案为:5;5NA.
点评:本题考查了原子结构示意图、原子的表示方法、电子数的求算、物质的量的有关计算等,题目考查的知识点较多,侧重于基础知识的考查,难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
下图是某些实验的部分装置,其中所注明的实验能达到实验目的是( )
A、 除去CO气体中的CO2气体 |
B、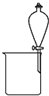 分离碘酒中的碘和酒精 |
C、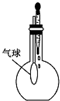 验证NH3的溶解性 |
D、 比较Na2CO3、NaHCO3的热稳定性 |
我们生活在五彩缤纷的世界里,以下色彩是由化学变化呈现出来的是( )
| A、雨后彩虹 | B、彩色图画 |
| C、节日焰火 | D、铜绿 |
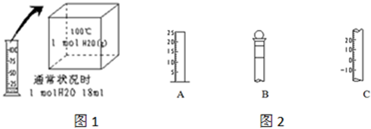
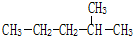


 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )