题目内容
在相同条件下,与0.5mol由N2和CO组成的混合气具有相同的体积的是( )
| A、1g H2 |
| B、10g O2 |
| C、11g CO2 |
| D、16g CH4 |
考点:物质的量的相关计算
专题:计算题
分析:在相同条件下,与0.5mol由N2和CO组成的混合气的物质的量相等的气体,体积也相等,根据n=
计算各气体的物质的量,判断各气体的物质的量是否为0.5mol.
| m |
| M |
解答:
解:A、1gH2的物质的量为:n(H2)=
=0.5mol,与0.5mol由N2和CO组成的混合气的物质的量相等,体积也相等,故A正确;
B、10gO2的物质的量为:n(O2)=
=0.3125mol,与0.5mol由N2和CO组成的混合气的物质的量不相等,则体积不相等,故B错误;
C、11gCO2的物质的量为:n(CO2)=
=0.25mol,与0.5mol由N2和CO组成的混合气的物质的量不相等,则体积不相等,故C错误;
D、16gCH4的物质的量为:n(CH4)=
=1mol,与0.5mol由N2和CO组成的混合气的物质的量不相等,则体积不相等,故D错误.
故选A.
| 1g |
| 2g/mol |
B、10gO2的物质的量为:n(O2)=
| 10g |
| 32g/mol |
C、11gCO2的物质的量为:n(CO2)=
| 11g |
| 44g/mol |
D、16gCH4的物质的量为:n(CH4)=
| 16g |
| 16g/mol |
故选A.
点评:本题考查阿伏加德罗定律及推论、物质的量的计算,题目难度不大,注意在相同条件下,物质的量相等的气体,体积也相等.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| C、0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA |
| D、将0.1mol Cl2与足量NaOH溶液在常温下充分反应,转移的电子数为0.1NA |
某学生做完实验以后,采用以下方法分别清洗所用仪器:
(1)用稀硝酸清洗做过银镜反应的试管;
(2)用酒精清洗做过碘升华的烧杯;
(3)用浓盐酸清洗做过高锰酸钾分解实验的试管;
(4)用盐酸清洗长期存放过三氯化铁溶液的试剂瓶;
(5)用氢氧化钠溶液清洗盛过苯酚的试管.
你认为他的操作( )
(1)用稀硝酸清洗做过银镜反应的试管;
(2)用酒精清洗做过碘升华的烧杯;
(3)用浓盐酸清洗做过高锰酸钾分解实验的试管;
(4)用盐酸清洗长期存放过三氯化铁溶液的试剂瓶;
(5)用氢氧化钠溶液清洗盛过苯酚的试管.
你认为他的操作( )
| A、(2)不对 |
| B、(3)、(4)不对 |
| C、(4)、(5)不对 |
| D、全部正确 |
俗话说“雷雨发庄稼”.在雷雨天,空气中有O3(由O2生成)和NO产生,下列说法正确的是( )
| A、NO在空气中不能稳定存在,会继续反应 |
| B、生成O3和NO的反应都是氧化还原反应 |
| C、O3和O2两种气体都是氧元素形成的单质,化学性质相同 |
| D、NO的产生是形成酸雨的主要原因 |
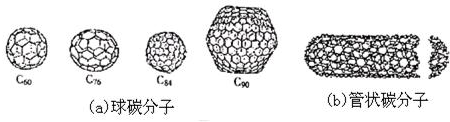
80年代中期,科学家发现并证明碳还以新的单质形态C60存在.后来人们又相继得到了C70、C76、C84、C90、C94等另外一些球碳分子.90年代初,科学家又发现了管状碳分子和洋葱状碳分子(如图).下列说法错误的是( )

| A、金刚石和石墨的熔点肯定要比C60高 |
| B、据估计C60熔点比金刚石和石墨要高 |
| C、无论是球碳分子,还是管状碳分子、洋葱状碳分子,都应看作是碳的同素异形体 |
| D、球碳分子是碳的同素异形体 |
VmL Al2(SO4)3溶液中,含有Al3+a g,取
mL溶液稀释到3V mL,则稀释后溶液中
的物质的量浓度是( )
| V |
| 2 |
| SO | 2- 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各组物质互为同分异构体的是( )
| A、H2O和H2O2 |
| B、己烷与环己烷 |
C、 与CH3CH2CH2CH3 与CH3CH2CH2CH3 |
| D、氰酸铵NH4CNO与尿素CO(NH2)2 |
燃烧某混合气体,所产生的CO2的质量一定大于燃烧相同质量乙烯所产生的CO2的量,该混合气体是( )
| A、乙烯、丙烷 |
| B、苯、乙烯 |
| C、甲烷、丙烷 |
| D、乙烷、环丙烷(C3H6) |
下列物质在空气中露置容易变质的是( )
| A、NaCl |
| B、CaCO3 |
| C、NaOH |
| D、KNO3 |