题目内容
常温下,下列关系的表述中,正确的是( )
| A、中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为l:l |
| B、pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)相等 |
| C、0.1 mol?L-NaHC03溶液中:c(Na+)>c(HCO3-)>c(CO32一)>c(H2C03) |
| D、浓度均为0.1 mol/L的三种溶液:①CH3COOH溶液;②NaOH溶液;⑧CH3COONa溶液,溶液的PH ②>③>① |
考点:离子浓度大小的比较,弱电解质在水溶液中的电离平衡,pH的简单计算,盐类水解的应用
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.醋酸为弱酸,等pH时,浓度较大;
B.盐酸抑制水的电离,氯化铁促进水的电离;
C.NaHC03溶液水解呈碱性,HCO3-水解大于电离程度;
D.按照等浓度时pH:强碱>弱碱>水解呈碱性>中性>水解呈酸性>酸的顺序比较.
B.盐酸抑制水的电离,氯化铁促进水的电离;
C.NaHC03溶液水解呈碱性,HCO3-水解大于电离程度;
D.按照等浓度时pH:强碱>弱碱>水解呈碱性>中性>水解呈酸性>酸的顺序比较.
解答:
解:A.醋酸为弱酸,等pH时,浓度较大,则醋酸消耗的氢氧化钠较多,故A错误;
B.盐酸抑制水的电离,氯化铁促进水的电离,故B错误;
C.NaHC03溶液水解呈碱性,HCO3-水解大于电离程度,则c(H2C03)>c(CO32一),故C错误;
D.等浓度时NaOH溶液pH最大,而①CH3COOH溶液呈酸性,则pH最小,所以溶液的PH ②>③>①,故D正确.
故选D.
B.盐酸抑制水的电离,氯化铁促进水的电离,故B错误;
C.NaHC03溶液水解呈碱性,HCO3-水解大于电离程度,则c(H2C03)>c(CO32一),故C错误;
D.等浓度时NaOH溶液pH最大,而①CH3COOH溶液呈酸性,则pH最小,所以溶液的PH ②>③>①,故D正确.
故选D.
点评:本题考查较为综合,涉及弱电解质的电离、盐类的水解等知识,侧重于学生的分析能力的考查,注意把握弱电解质的电离和盐类水解的原理,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
在一定条件下,2NO+O2?2NO2达到平衡的标志是( )
| A、NO、O2、NO2分子数目比是2:1:2 |
| B、反应混合物中各组分物质的浓度相等 |
| C、混合气体的颜色不再变化 |
| D、混合气体的平均相对分子质量改变 |
在H2SO4和Al2(SO4)3的混合溶液中,铝离子浓度是0.4mol/L,硫酸根离子浓度是0.7mol/L,则氢离子浓度最接近于( )
| A、0.1 mol/L |
| B、0.2 mol/L |
| C、0.3 mol/L |
| D、0.4 mol/L |
下列反应的离子方程式正确的是( )
| A、硫酸氢钠溶液中滴入Ba(OH)2溶液使所得溶液呈中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| B、成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H2O |
| C、向苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| D、向碱性KMnO4溶液中滴加HCOOK溶液:2MnO4-+HCOO-+OH-═MnO42-+CO2↑+H2O |
下列说法中,正确的是( )
| A、钠、钾着火时可用水灭火 |
| B、面粉厂或加油站不必严禁烟火 |
| C、氨气泄漏时可喷洒大量水进行处理 |
| D、节日期间可在人群聚集的闹市燃放烟花爆竹 |
下列对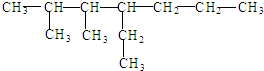 的命名中正确的是( )
的命名中正确的是( )
 的命名中正确的是( )
的命名中正确的是( )| A、2,3-二甲基-4-丙基己烷 |
| B、2,3-二甲基-4-乙基庚烷 |
| C、4-乙基-2,3-二甲基庚烷 |
| D、5,6-二甲基-4-乙基庚烷 |

