题目内容
在标准状况下,将质量为相同状况下同体积氢气质量16倍的CO2和CO的混合气体,充满盛有Na2O2且容积为(1)反应前充入容器中的CO2和CO的物质的量各是多少?
(2)最后容器中的生成物有哪些?其质量各是多少?
(1)n(CO2)=0.025 mol,n(CO)=0.075 mol
(2)生成物为Na2CO3和O2;其中Na2CO3为
解析:由题意知混合气体的平均相对分子质量为16×2=32,
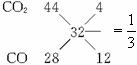 ,故n(CO2)=
,故n(CO2)=![]() ×0.1 mol=0.025 mol,n(CO)=0.075 mol,又因:2CO2+2Na2O2
×0.1 mol=0.025 mol,n(CO)=0.075 mol,又因:2CO2+2Na2O2![]() 2Na2CO3+O2,2CO+O2
2Na2CO3+O2,2CO+O2![]() 2CO2,可看作按CO+Na2O2
2CO2,可看作按CO+Na2O2![]() Na2CO3和2CO2+2Na2O2
Na2CO3和2CO2+2Na2O2![]() 2Na2CO3+O2两反应进行,CO完全消耗掉,生成的O2可由CO2与Na2O2的反应求得,故由C原子守恒知:生成Na2CO3为0.1 mol,产生O2共0.025 mol×
2Na2CO3+O2两反应进行,CO完全消耗掉,生成的O2可由CO2与Na2O2的反应求得,故由C原子守恒知:生成Na2CO3为0.1 mol,产生O2共0.025 mol×![]() =0.012 5 mol。
=0.012 5 mol。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
在标准状况下,将SO2,HCl,H2组成的混和气体4.48L通过足量的NaOH溶液,溶液的质量增加6.85g,从溶液中逸出的气体经干燥后体积为1.12L,则原混和气体中 SO2的体积为( )
| A、0.224 L | B、1.12 L | C、3、36L. | D、4L |