题目内容
7. 某溶液中含有Ba2+,Mg2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(已知溶液2为无色溶液)
某溶液中含有Ba2+,Mg2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(已知溶液2为无色溶液)(1)沉淀的化学式:沉淀1:AgCl,沉淀2:BaSO4或Mg(OH)2;沉淀3:Mg(OH)2或BaSO4.
(2)写出“混合液+A”的离子方程式:Ag++Cl-=AgCl↓;“生成沉淀2”的离子方程式Ba2++SO42-=BaSO4↓或Mg2++2OH-=Mg(OH)2↓.
(3)从溶液1和B反应后分离得到沉淀2和溶液2的实验中,使用到的玻璃仪器有漏斗、玻璃棒、烧杯.
分析 由分离流程可知,溶液含有Ba2+、Mg2+、Ag+,应先加A为入HCl,生成沉淀1为AgCl,过滤后溶液1中加试剂B为Na2SO4,可得到沉淀2为BaSO4,最后溶液2中加入试剂C为NaOH,可得到沉淀3为Mg(OH)2,或过滤后溶液1中加试剂B为NaOH,可得到沉淀2为Mg(OH)2,最后溶液2中加入试剂C为Na2SO4,可得到沉淀3为BaSO4,均符合溶液2为无色溶液,以此来解答.
解答 解:(1)由上述分析可知,沉淀1为AgCl,沉淀2为BaSO4或Mg(OH)2,沉淀3为Mg(OH)2或BaSO4,
故答案为:AgCl;BaSO4或Mg(OH)2;
(2)“混合液+A”的离子方程式为Ag++Cl-=AgCl↓;“生成沉淀2”的离子方程式为Ba2++SO42-=BaSO4↓或Mg2++2OH-=Mg (OH)2↓,
故答案为:Ag++Cl-=AgCl↓;Ba2++SO42-=BaSO4↓或Mg2++2OH-=Mg (OH)2↓;
(3)从溶液1和B反应后分离得到沉淀2和溶液2的实验操作为过滤,使用到的玻璃仪器有漏斗、玻璃棒、烧杯,
故答案为:漏斗、玻璃棒、烧杯.
点评 本题考查混合物分离,为高频考点,把握离子的性质、发生的反应及混合物分离为解答的关键,侧重分析与应用能力的考查,注意离子逐一沉淀的限制条件,题目难度不大.

练习册系列答案
相关题目
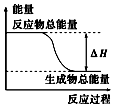
7.下列物质间的反应,其能量变化符合如图所示的是( )

| A. | 铝粉与氧化铁在加热条件下的反应 | |
| B. | 灼热的碳与二氧化碳反应 | |
| C. | Ba(OH)2•8H2O晶体和NH4Cl晶体混合 | |
| D. | 碳与水高温条件下制取水煤气的反应 |
18.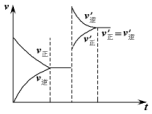 如图表示在密闭容器中反应C(s)+H2O(g)$\stackrel{高温}{?}$CO(g)+H2(g);△H>0,达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况.据图可知,改变的条件是( )
如图表示在密闭容器中反应C(s)+H2O(g)$\stackrel{高温}{?}$CO(g)+H2(g);△H>0,达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况.据图可知,改变的条件是( )
 如图表示在密闭容器中反应C(s)+H2O(g)$\stackrel{高温}{?}$CO(g)+H2(g);△H>0,达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况.据图可知,改变的条件是( )
如图表示在密闭容器中反应C(s)+H2O(g)$\stackrel{高温}{?}$CO(g)+H2(g);△H>0,达到平衡后,由于条件的改变而引起正、逆反应速率的变化,以及平衡移动的状况.据图可知,改变的条件是( )| A. | 增加CO浓度 | B. | 升高温度 | C. | 增加水蒸气 | D. | 增大压强 |
15.关于物质的类别,下列说法正确的是( )
| A. | 食盐水、糖水、冰水都属于混合物 | |
| B. | 烧碱、火碱、消石灰都属于碱 | |
| C. | KHSO4、HCl、HNO3在水中都能电离出氢离子,都属于酸 | |
| D. | 溶液、胶体、浊液都属于稳定的分散系 |
12.下列离子方程式书写正确的是( )
| A. | CuSO4溶液与Ba (OH)2溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | NaHSO4溶液和NaHCO3溶液反应:H++HCO3-═H2O+CO2↑ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 往BaCl2溶液中通入少量的SO2:Ba2++SO2+H2O═BaSO3↓+2H+ |
19.食品安全问题备受人们关注,但应该区别违法食品添加剂与正常食品添加剂.做馒头的过程中禁止添加的是( )
| A. | 小苏打 | B. | 增白剂 | C. | 蔗糖 | D. | 食盐 |
15.下列说法中正确的是( )
| A. | 标准状况下,22.4L水中所含的分子数约为6.02×1023 | |
| B. | 标准状况下,aL的氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$×6.02×1023 | |
| C. | 常温常压下,48g O3气体含有的氧原子数为6.02×1023 | |
| D. | 1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |