题目内容
18.下列说法正确的是( )| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | 1.00 mol NaCl中含有6.02×1023个NaCl分子 | |
| D. | 纯净矿泉水、铝热剂、漂白粉均为混合物 |
分析 A.NaC1O是强电解质;
B.HCl为共价化合物;
C.从氯化钠是离子混合物分析判断;
D.由多种物质组成的属于混合物.
解答 解:A.NaC1O是盐,属于强电解质,故A错误;
B.HCl为共价化合物,故B错误;
C.氯化钠是离子化合物,在常温下无氯化钠分子存在,故C错误;
D.纯净矿泉水、铝热剂、漂白粉均为多种物质组成的混合物,故D正确,故选D.
点评 本题考查较为综合,涉及电解质、强弱电解质、共价化合物以及混合物等知识,为高考常见题型,侧重于学生的分析能力的考查,题目较为基础,贴近高考,有利于培养学生良好的科学素养,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
6.室温下,pH均为12的两种溶液:①氨水.②氢氧化钠溶液.下列说法不正确的是( )
| A. | 两溶液中c(OH-):①=② | |
| B. | 两溶液的物质的量浓度:①=② | |
| C. | 两溶液分别加水稀释10倍,稀释后溶液的pH:①>② | |
| D. | 等体积的两溶液分别与同浓度的盐酸完全中和,消耗盐酸的体积:①>② |
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24LCl2溶于足量水中转移电子的数目为0.1NA | |
| B. | 标准状况下,22.4L苯中含有双键的数目为3NA | |
| C. | 常温下,16gO2和O3的混合气体中含有氧原子的数目为NA | |
| D. | 25℃时,pH=1的醋酸溶液中含有H+的数目为0.1NA |
3.已知化学反应①:
Fe(s)+CO2(g)═FeO(s)+CO(g),其平衡常数为K1;化学反应②:
Fe(s)+H2O(g)═FeO(s)+H2(g),其平衡常数为K2.在温度
973K和1173K情况下,K1、K2的值分别如下:
(1)通过表格中的数值可以推断:反应①是吸热(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.据此关系式及上表数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有DF(填写序号).
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
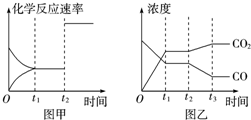
(4)图甲、乙分别表示反应③在t1时刻达到平衡、在t2时刻因改变某个条件而发生变化的情况:
①图甲中t2时刻发生改变的条件是加入催化剂或增大体系的压强.
②图乙中t2时刻发生改变的条件是降低温度或增加水蒸气的量或减少氢气的量.
Fe(s)+CO2(g)═FeO(s)+CO(g),其平衡常数为K1;化学反应②:
Fe(s)+H2O(g)═FeO(s)+H2(g),其平衡常数为K2.在温度
973K和1173K情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.据此关系式及上表数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有DF(填写序号).
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
(4)图甲、乙分别表示反应③在t1时刻达到平衡、在t2时刻因改变某个条件而发生变化的情况:
①图甲中t2时刻发生改变的条件是加入催化剂或增大体系的压强.
②图乙中t2时刻发生改变的条件是降低温度或增加水蒸气的量或减少氢气的量.

10.“预防污染”要求我们利用各种手段减少各种污染物的排放,提高资源和能源的利用效率,绿色化学是“预防污染”的基本手段,下列各项中属于绿色化学的是( )
| A. | 处理废弃物 | B. | 治理污染点 | C. | 减少有毒物排放 | D. | 杜绝污染源 |
7.下列关于物质性质的说法不正确的是( )
| A. | 通常状况下,NO2是红棕色的气体 | |
| B. | 氯水光照久置后最终变为稀盐酸 | |
| C. | 氯化钙溶液和AgNO3溶液混合有白色沉淀产生 | |
| D. | 加热时,铁单质与浓硝酸不发生反应 |
8.下列金属最易与H2O发生反应的是( )
| A. | Na | B. | K | C. | Al | D. | Mg |
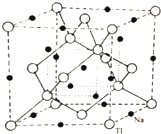 ⅢA族的硼、铝、镓、铟、铊等元素在化合物中通常表现出+3价,含ⅢA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题.
ⅢA族的硼、铝、镓、铟、铊等元素在化合物中通常表现出+3价,含ⅢA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题.
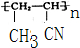
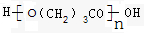
 .
.