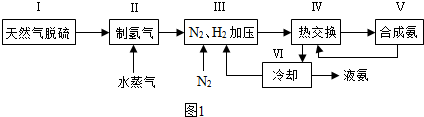
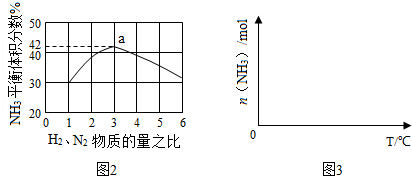
题目内容
下列实验操作正确且能达到预期目的是( )
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入酸性KMnO4溶液,看紫红色是否褪去 |
| C | 确定碳、氯两元素非金属性的强弱 | 测定同温同浓度的Na2CO3和NaClO水溶液的pH |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,非金属在元素周期表中的位置及其性质递变的规律,苯酚的化学性质,物质的分离、提纯和除杂,有机物(官能团)的检验
专题:实验评价题,有机物的化学性质及推断
分析:A.可根据乙醇、水分别与钠反应的剧烈程度比较;
B.碳碳双键和醛基都可被酸性高锰酸钾氧化;
C.应用最高价氧化物对应的水化物的盐溶液;
D.溴、三溴苯酚都溶液苯中.
B.碳碳双键和醛基都可被酸性高锰酸钾氧化;
C.应用最高价氧化物对应的水化物的盐溶液;
D.溴、三溴苯酚都溶液苯中.
解答:
解:A.乙醇、水都可与钠反应,但反应的剧烈程度不同,可根据反应的剧烈程度比较,故A正确;
B.碳碳双键和醛基都可被酸性高锰酸钾氧化,应先发生银镜反应,然后在用酸性高锰酸钾溶液检验,故B错误;
C.应用最高价氧化物对应的水化物的盐溶液,不能用NaClO,故C错误;
D.苯酚和溴发生取代反应生成三溴苯酚,溴、三溴苯酚都溶液苯中,应用氢氧化钠溶液除杂,故D错误.
故选A.
B.碳碳双键和醛基都可被酸性高锰酸钾氧化,应先发生银镜反应,然后在用酸性高锰酸钾溶液检验,故B错误;
C.应用最高价氧化物对应的水化物的盐溶液,不能用NaClO,故C错误;
D.苯酚和溴发生取代反应生成三溴苯酚,溴、三溴苯酚都溶液苯中,应用氢氧化钠溶液除杂,故D错误.
故选A.
点评:本题考查有机物的鉴别、性质比较以及物质的分离、除杂等,为高频考点,选项B为解答的难点,侧重有机物鉴别及有机反应的考查,综合性较强,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
金属材料有着广泛的应用.下列说法错误的是( )
| A、用热碱液清洗铝材表面的油污时,会有气泡冒出 |
| B、电解精炼铜,电解结束后电解液浓度不变 |
| C、Fe2+、H+、NO3-三者不共存的原因为:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
| D、硬铝是以铝为主要合金元素的合金材料,其熔点低于纯铝 |
下列有关实验的叙述正确的是( )
| A、用浓硝酸做试剂比较铁和铜的金属活动性 |
| B、用干燥洁净的玻璃棒蘸取氯水滴在干燥PH试纸上,测定氯水的PH |
| C、向两只分别装有碳酸钠和碳酸氢钠固体的试管中各加几滴水,前者温度降低,后者温度升高 |
| D、欲检验Br-的存在,可在溶液中先加入氯水,再加入CCl4,振荡、静置,观察下层溶液是否出现橙红色 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温下,9g H2O中含NA个O-H键 |
| B、1mol Fe2+与足量稀硝酸反应,转移3NA个电子 |
| C、常温常压下,22.4L SO2和O2的混合气体中含2NA个氧原子 |
| D、0.1mol?L-1 KAl(SO4)2溶液中含0.2NA个SO42- |
能达到实验目的是( )
A、 称NaOH固体的质量 |
B、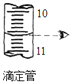 读数为10.60 |
C、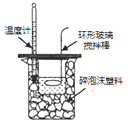 反应热的测定 |
D、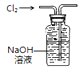 收集氯气 |